Cell | 面向药物发现的新方法学范式
Cell | 面向药物发现的新方法学范式

DrugAI
发布于 2026-04-13 15:45:26
发布于 2026-04-13 15:45:26
DRUGONE
传统以动物模型为核心的药物研发体系长期面临极高的失败率,这促使研究人员不断探索更加以人为中心的新方法学(NAMs)。近年来,基于干细胞、类器官以及计算模型的技术迅速发展,并在监管政策的推动下,逐渐覆盖从疾病建模、药物设计到疗效评估的整个药物发现流程。
本综述系统总结了这些新方法学在多个关键领域的进展,包括候选药物的发现、先进模型与技术的发展,以及NAMs在临床前和临床阶段作为治疗手段的潜力。同时,研究人员也分析了限制其广泛应用的关键瓶颈,包括生物学复杂性、技术挑战以及监管问题。综述最后强调了在推动NAMs转化应用过程中需要考虑的社会与伦理问题,并展望了未来以人为中心的药物研发体系将如何重塑整个领域。

药物研发一直是一个高风险过程,超过90%的候选药物在临床阶段失败。其中,疗效不足和毒性问题是主要原因,而这些问题很大程度上源于动物模型与人体之间的生物差异,以及现有模型无法真实反映人类疾病的复杂性。
这一局限性促使研究人员重新思考传统动物实验的可靠性,并推动监管机构逐步转向以人为中心的替代方法。美国FDA和NIH近年来在政策层面持续推进这一转型,从允许替代动物实验,到引入人工智能与真实世界数据,逐步构建新的药物研发范式。
与此同时,技术层面的进步也在同步推进。干细胞技术使研究人员能够获得患者特异性的细胞来源,类器官技术提供了更接近真实组织结构的模型,而人工智能则进一步提升了药物设计和毒性预测能力。这些技术的融合标志着药物研发正在从“动物驱动”转向“人类驱动”的新阶段。
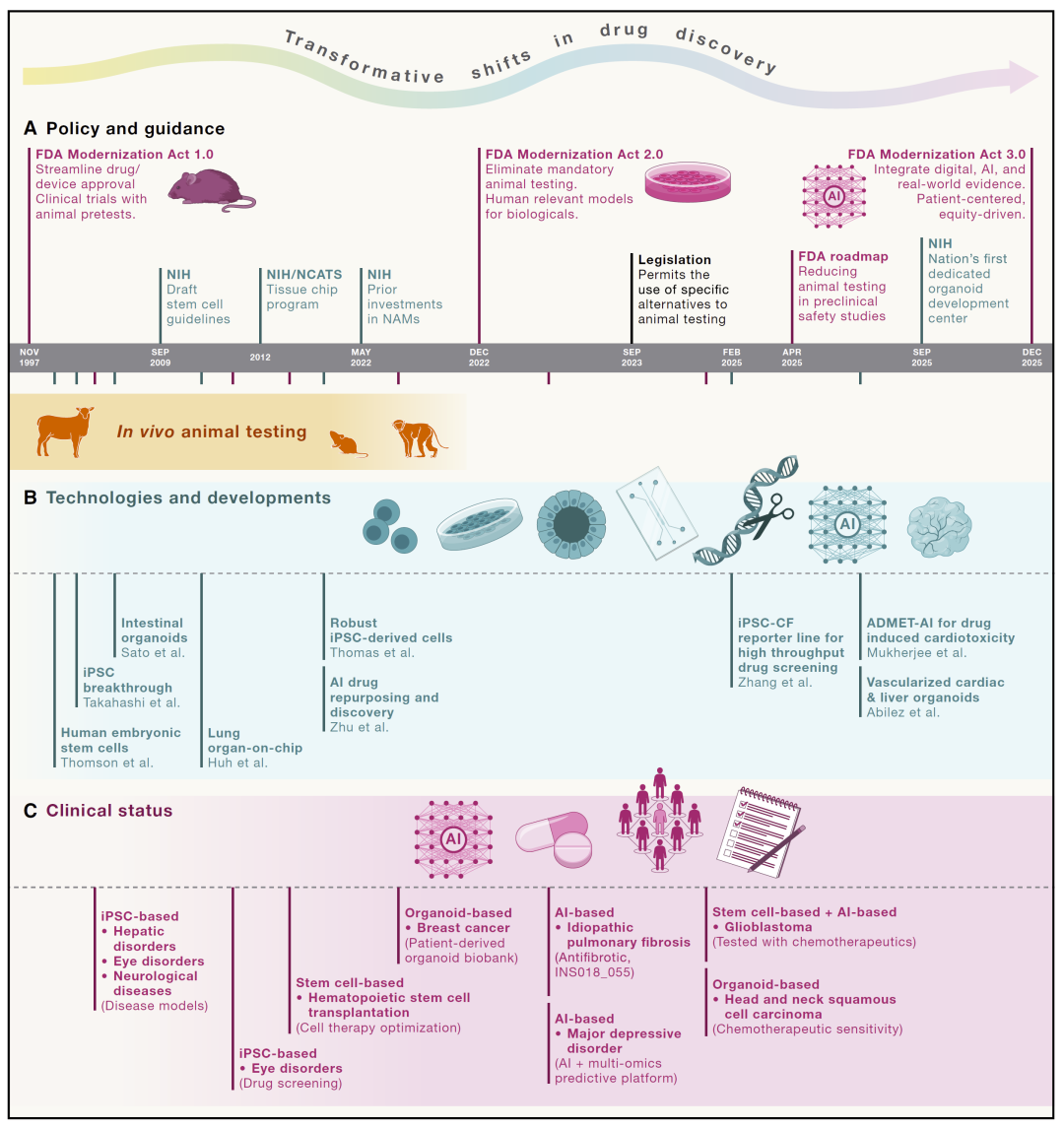
图1:药物发现范式转变的时间轴。
2D干细胞基础NAMs:细胞层面的疾病建模与药物发现
干细胞技术为药物研发提供了全新的研究路径。人多能干细胞可以分化为几乎所有类型的人体细胞,使研究人员能够在体外重建疾病相关细胞环境,从而更真实地模拟人类疾病。
这些模型不仅能够反映患者特异性的遗传背景,还能够再现动物模型难以捕捉的疾病表型。例如,在神经退行性疾病、心血管疾病以及肝脏疾病等领域,干细胞模型已经成功揭示了关键致病机制,并发现多个潜在治疗靶点。
在过去几年中,这些平台被广泛应用于不同器官系统的研究。从神经系统到心脏、血管以及代谢器官,研究人员利用干细胞模型系统性地筛选药物候选物,并解析其作用机制。这些成果表明,干细胞NAMs不仅是描述性模型,更逐渐成为预测性与机制性工具。
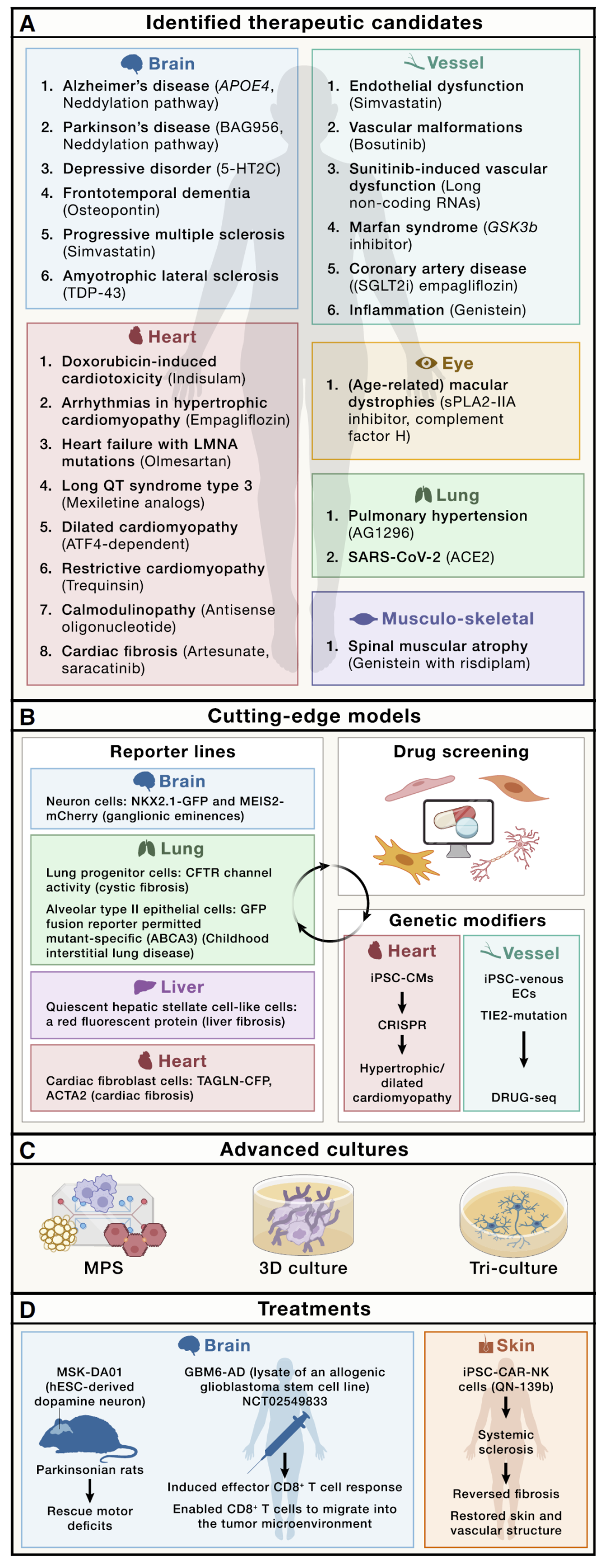
图2:细胞层面的NAMs:基于患者来源iPSC的筛选平台。
进一步发展中,干细胞平台还衍生出多种先进技术,例如报告基因系统、高通量筛选以及基因编辑工具。这些技术能够在细胞水平上实现精确的功能解析,并加速药物筛选流程。同时,多细胞共培养系统和微生理系统的引入,使模型能够更真实地模拟组织间相互作用。
此外,干细胞不仅用于疾病建模,也逐渐成为治疗手段的一部分。例如干细胞衍生细胞在神经系统疾病、免疫疾病以及肿瘤治疗中的应用,显示出良好的转化潜力。这种从“模型”到“治疗”的转变,体现了NAMs的独特优势。
尽管如此,这类模型仍面临成熟度不足、表型不稳定以及难以完全模拟复杂疾病等问题。因此,提高模型成熟度、增强多细胞互作以及建立标准化体系,是未来发展的关键方向。
3D类器官基础NAMs:组织与器官层面的功能建模
在干细胞模型基础上,类器官技术进一步提升了生理相关性。通过构建三维结构并整合多种细胞类型,类器官能够在体外模拟真实器官的结构与功能。
这些模型已被广泛应用于多个领域。在肿瘤研究中,类器官能够保留患者肿瘤的遗传特征和表型特征,从而用于药物筛选和个体化治疗。在感染性疾病、代谢疾病以及神经系统疾病中,类器官同样展现出强大的建模能力。
在药物发现方面,类器官不仅能够识别潜在治疗候选物,还能够评估其在复杂组织环境中的作用效果。这使得药物筛选更加接近真实临床场景。
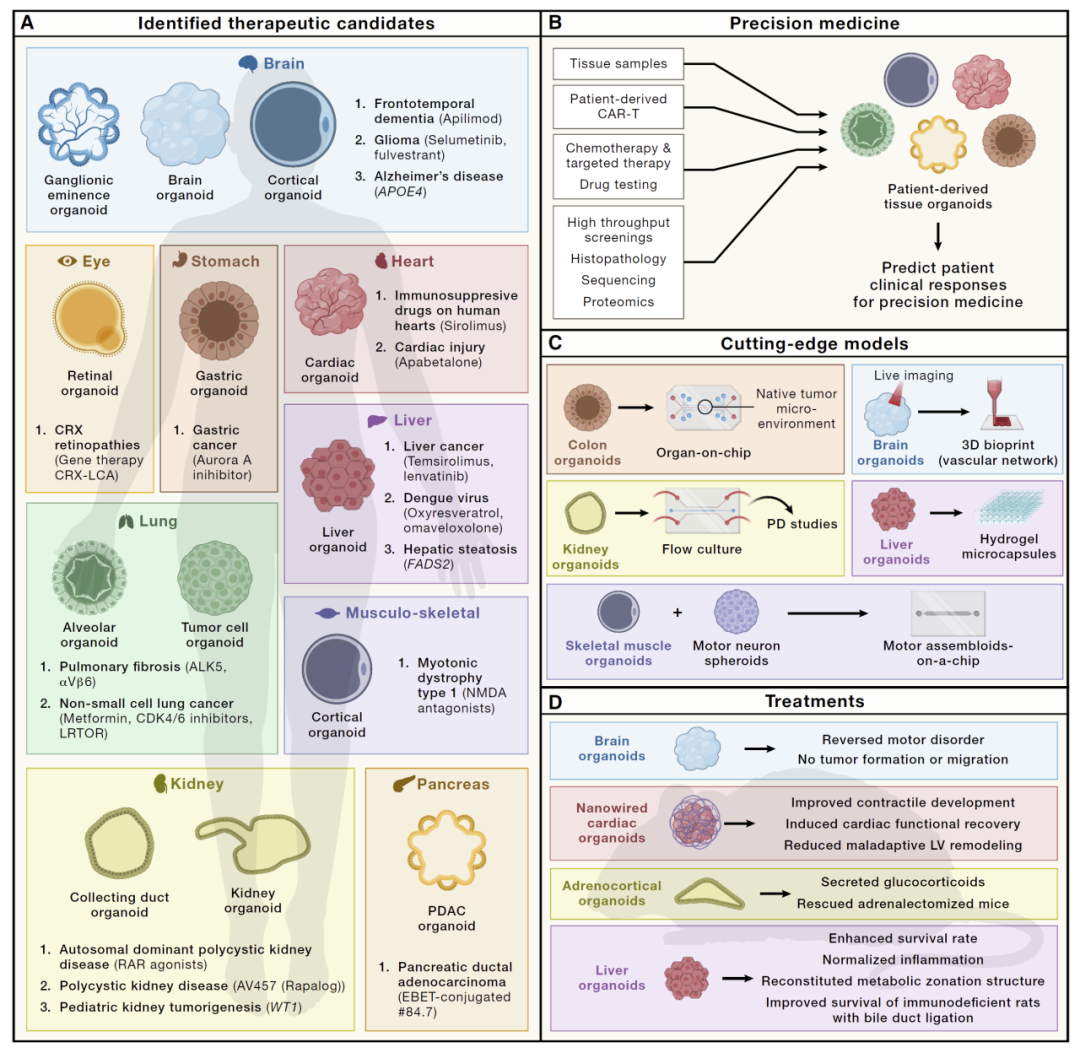
图3:多细胞层面的NAMs:用于人类组织建模的类器官平台。
此外,类器官正在成为精准医学的重要工具。通过患者来源的类器官,研究人员可以在体外测试不同治疗方案,并预测患者的临床反应。这种“个体化药物筛选”模式,有望显著提高治疗成功率。
与此同时,工程化技术进一步推动类器官发展。例如器官芯片、三维打印以及血管化技术,使模型更加复杂和真实。这些进展正在缩小体外模型与人体之间的差距。
尽管取得显著进展,类器官仍面临一些挑战,包括缺乏血管系统、成熟度不足以及微环境模拟不完整等问题。未来需要通过多技术融合来解决这些限制。
计算与AI驱动NAMs:数据与模型层面的革命
随着数据规模的扩大,计算方法在药物研发中的作用日益突出。基于人工智能的模型可以从大规模数据中学习复杂规律,从而用于药物设计、靶点发现以及毒性预测。
AI方法不仅能够加速候选药物筛选,还可以通过多组学数据整合,实现更精准的疾病理解。同时,生成模型和预测模型的发展,使药物设计从经验驱动转向数据驱动。
这些计算方法通常与实验平台结合使用,例如与干细胞和类器官模型联动,从而形成闭环优化系统。这种“计算+实验”的协同模式,显著提升了研发效率。
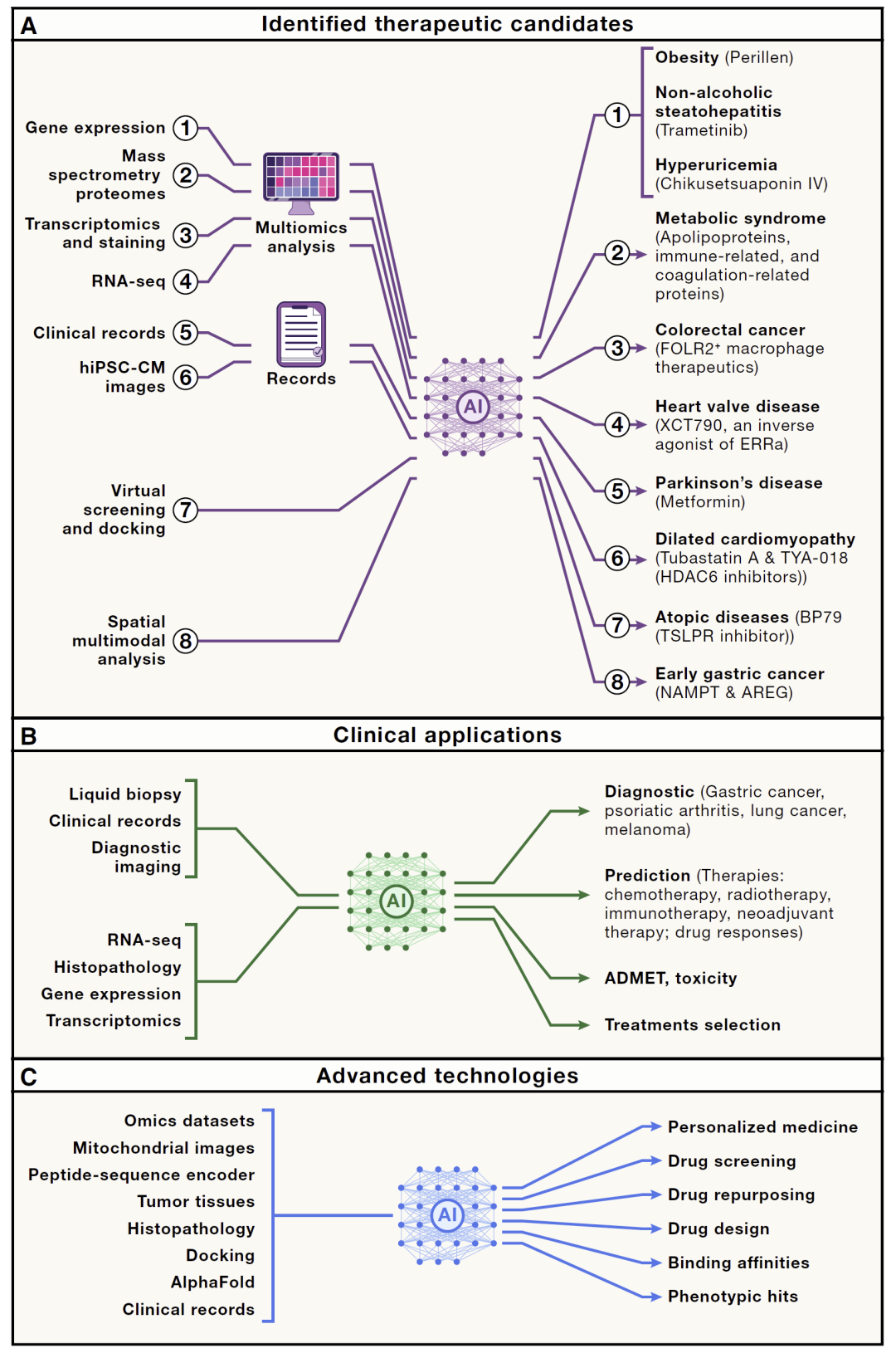
图4:计算层面的NAMs:预测性药物发现的工作流程。
NAMs在临床转化中的应用
随着技术成熟,NAMs正在逐步进入临床研究阶段。从干细胞治疗到类器官辅助药物筛选,再到AI驱动的诊断工具,这些方法正在改变临床研究模式。
例如,患者来源模型被用于指导个体化治疗方案,而AI模型则用于预测疾病进展和治疗反应。这些应用表明,NAMs不仅能够改进药物发现,还能够直接影响临床决策。
此外,一些完全基于NAMs的研究已经获得监管认可,表明其在替代传统动物实验方面具有潜力。这一趋势将进一步推动以人为中心的药物研发体系。
讨论与展望
本综述系统展示了NAMs在药物研发中的重要作用,并强调其正在推动整个领域发生范式转变。从细胞层面到器官层面,再到计算模型,NAMs构建了一个多层次的人类中心研究体系。
然而,要实现其全面应用,仍需解决多个关键问题,包括模型标准化、跨平台整合以及监管体系完善。此外,数据共享、伦理问题以及成本控制也将成为未来发展的重要考量。
展望未来,随着技术不断成熟和政策支持加强,NAMs有望逐步取代传统动物模型,构建更加高效、精准和可持续的药物研发体系。这一转变不仅将提高新药研发成功率,也将深刻改变生物医学研究的整体格局。
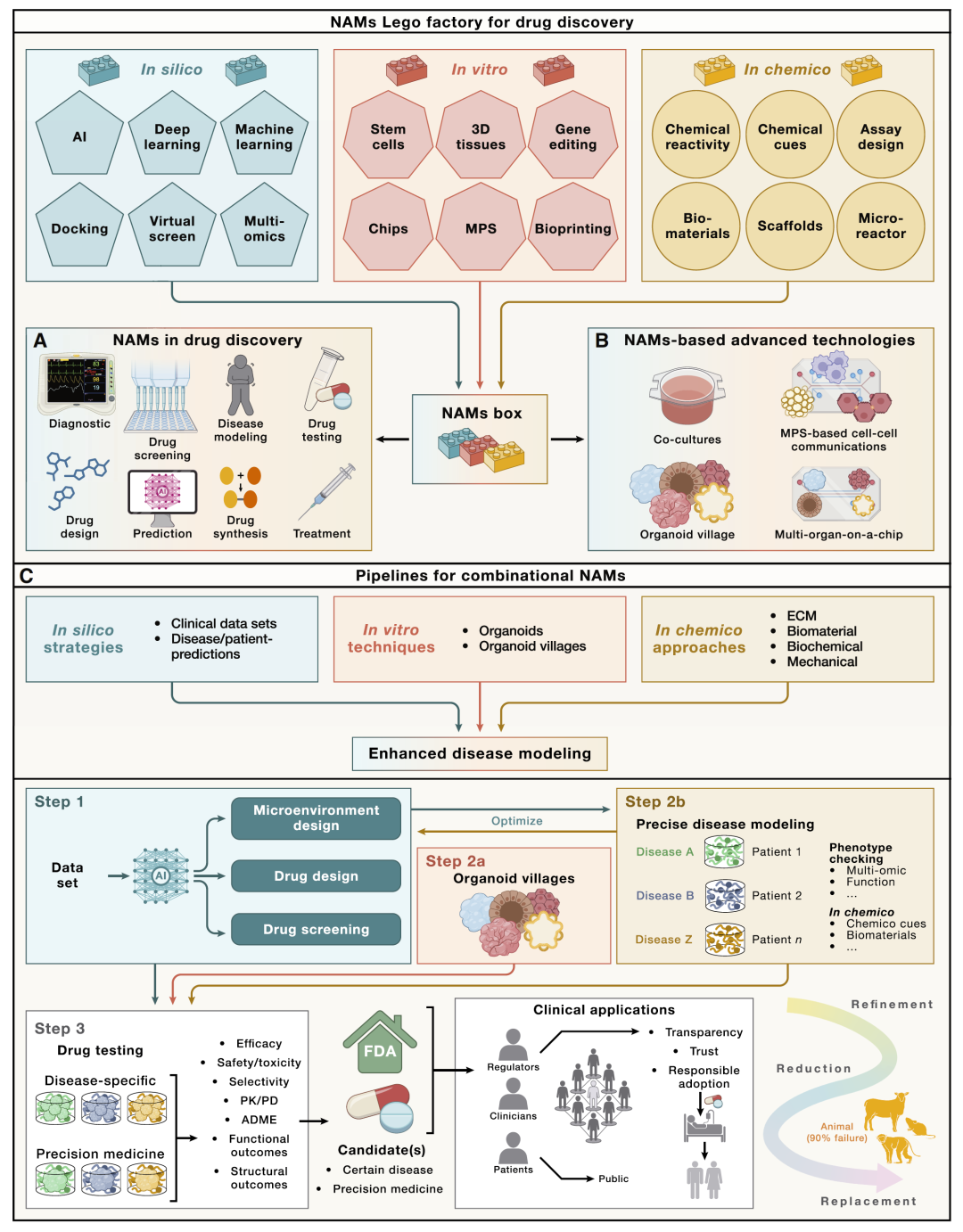
图5:基于NAMs的人类中心化药物发现集成流程。
整理 | DrugOne团队
参考资料
Liu, W., Pang, P.D., Wu, C.A., Tagle, D. and Wu, J.C., 2026. New approach methodologies for drug discovery. Cell, 189(7), pp.1877-1903.

内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-07,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

