🧠 Nature | 单细胞+Xenium空间转录组+活细胞成像,三维度解析幕上室管膜瘤异质性全景图
🧠 Nature | 单细胞+Xenium空间转录组+活细胞成像,三维度解析幕上室管膜瘤异质性全景图

生信大杂烩
发布于 2026-04-13 18:18:47
发布于 2026-04-13 18:18:47

论文标题:Multidimensional profiling of heterogeneity in supratentorial ependymomas 发表期刊:Nature (2026) 通讯作者:Mariella G. Filbin(Dana-Farber / 哈佛大学) DOI:10.1038/s41586-026-10214-2
一、研究背景
脑肿瘤是儿童和青少年中癌症相关死亡的首要原因,其死亡率已超过白血病。幕上室管膜瘤(Supratentorial Ependymomas, ST-EPNs)是发生于中枢神经系统的一类恶性脑肿瘤,患者预后差异显著,且可用的治疗手段极为有限。
近年来,基于全基因组DNA甲基化谱的分类研究将ST-EPNs细分为多个分子亚型,包括:**(1) 经典ST-ZFTA亚型(以ZFTA-RELA融合基因为特征);(2) 非经典ST-ZFTA亚型**(ZFTA cluster 1-4,携带ZFTA-RELA或ZFTA与其他伙伴基因的融合);以及 (3) ST-YAP1亚型(富集YAP1融合)。不同亚型之间的预后和治疗反应存在明显差异,但其背后不同的细胞起源和恶性细胞状态组成仍不清楚。
此前的单细胞研究虽然初步揭示了ST-EPNs的细胞异质性,但存在两个关键局限:一是未涵盖非经典ST-ZFTA亚型,导致许多细胞状态是样本或亚型特异性的;二是缺失了空间信息,无法解析细胞状态在肿瘤组织中的空间组织模式及其与微环境的互作关系。
本研究的核心贡献在于首次整合单细胞/单核转录组学、10x Xenium空间转录组学以及体外/体内活细胞成像三大维度,系统性地解析了所有ST-EPN亚型的细胞状态、空间组织架构和动态行为特征,构建了一个多维度的肿瘤异质性分析框架。
二、研究设计:多维度整合分析策略
本研究的实验设计可概括为三个层次:
分析维度 | 技术平台 | 样本规模 | 核心目标 |
|---|---|---|---|
转录组学 | Smart-seq2 sc/snRNA-seq | 42份肿瘤样本(34位患者),7,046个恶性细胞 | 定义细胞状态与发育特征 |
空间组学 | 10x Genomics Xenium | 56个肿瘤切片(23位ZFTA-RELA患者),358个靶基因 | 解析空间组织模式 |
细胞行为学 | 体外共培养+体内PDX活细胞成像 | 3个患者来源细胞系(EP1NS, BT165, VBT242) | 表征形态和迁移行为 |
关键实验设计亮点包括:
- 全覆盖的亚型纳入:首次同时分析经典ZFTA-RELA和所有非经典ST-ZFTA亚型(cluster 1-4)
- Xenium定制探针panel:结合103个自定义基因和255个预设人脑基因panel,并设计了3种ZFTA-RELA融合特异性探针
- 多模型系统验证:使用单层/球状培养、大鼠E19皮质细胞共培养、PDX以及人iPSC来源神经元共培养进行交叉验证
三、主要发现
3.1 ST-EPN亚型的转录组特征映射到不同的发育时间窗口
研究者首先通过DNA甲基化分析确认了所有样本的亚型分类(Fig. 1b),随后对7,046个高质量恶性细胞进行了统一的低维空间共嵌入分析。
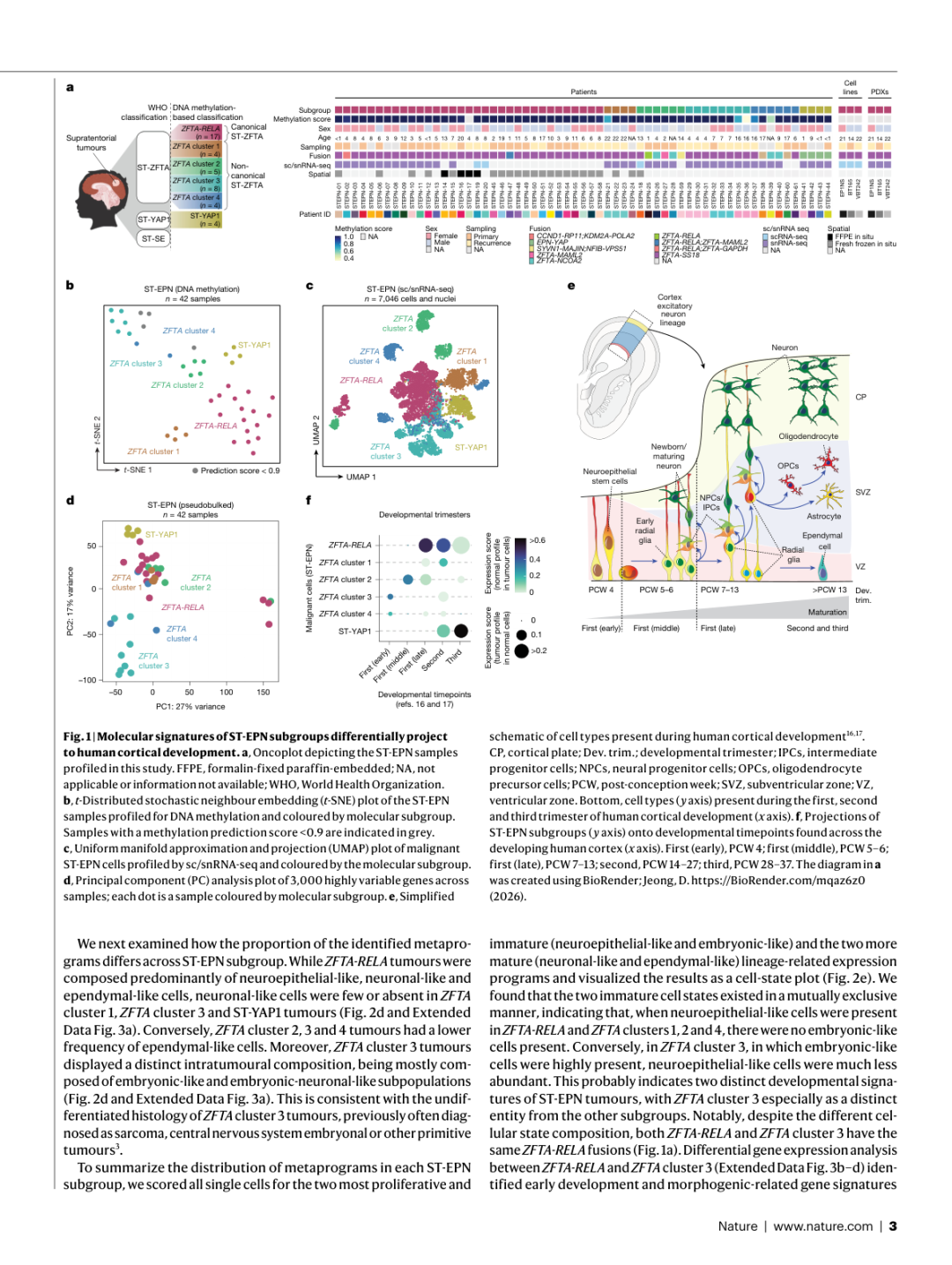
Figure 1: ST-EPN亚型的分子特征与发育时间窗口映射
Figure 1: ST-EPN亚型的分子特征与发育时间窗口映射
▲ Figure 1 | ST-EPN亚型的分子特征差异性映射到人类皮质发育的不同阶段。 (a) 研究队列Oncoplot;(b) DNA甲基化t-SNE分群;(c) sc/snRNA-seq UMAP展示恶性细胞按亚型聚类;(d) PCA分析显示样本按亚型分组;(e) 人类皮质发育参考图谱示意图;(f) 各ST-EPN亚型向发育时间窗口的投影。
核心发现:
- 恶性细胞按分子亚型明确聚类(Fig. 1c,d),表明不同亚型具有截然不同的转录组特征
- 通过构建人类大脑皮质发育图谱(整合PCW 4-37的两个公开scRNA-seq数据集),将各亚型的基因表达谱投射到发育时间轴上(Fig. 1f):
- ZFTA cluster 3/4 → 投射到最早期的发育窗口(早期和中期第一个三月期)
- ZFTA cluster 1/2 → 投射到中期第一和第二个三月期
- 经典ZFTA-RELA → 广泛投射从晚期第一到第三个三月期
- ST-YAP1 → 对齐到最晚的发育时间点
这一发现从发育生物学角度揭示了ST-EPN不同亚型的"发育年龄"差异:ZFTA cluster 3对应最原始的胚胎状态,而ST-YAP1对应最成熟的发育阶段,提示不同亚型可能起源于发育过程中不同阶段的前体细胞。
3.2 八种元程序定义了ST-EPN的瘤内异质性
接下来,研究者通过非负矩阵分解(NMF)在每个样本内独立地识别转录程序,然后通过层次聚类发现了8种跨样本的元程序(metaprograms),这些元程序定义了ST-EPN肿瘤内部的细胞状态多样性。
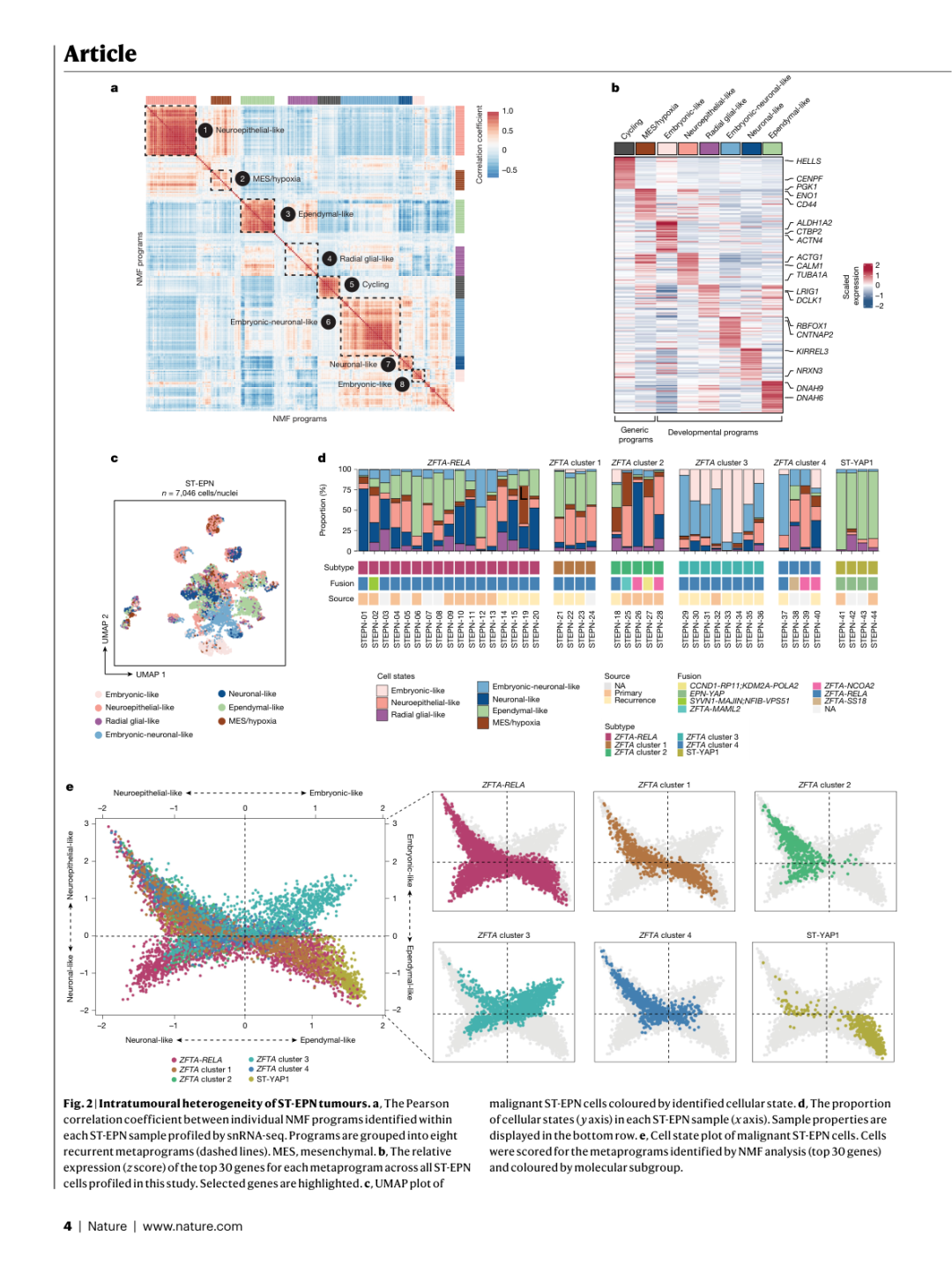
Figure 2: ST-EPN肿瘤的瘤内异质性
Figure 2: ST-EPN肿瘤的瘤内异质性
▲ Figure 2 | ST-EPN瘤内异质性的全景解析。 (a) NMF程序间的Pearson相关性矩阵,鉴定出8种元程序;(b) 各元程序的标志基因表达热图;(c) UMAP展示细胞状态分布;(d) 各样本中细胞状态的比例组成;(e) 细胞状态图展示祖细胞样与成熟谱系的分布。
八种元程序包括两类:
通用肿瘤程序(2种):
- 增殖型(Cycling):高表达HELLS、CENPF,富集细胞增殖相关基因
- 间质/低氧型(MES/hypoxia):高表达PGK1、ENO1、CD44,富集低氧相关基因
发育相关程序(6种):3. 胚胎样(Embryonic-like):高表达ALDH1A2、CTBP2、ACTN4,富集视黄酸受体信号通路 4. 神经上皮样(Neuroepithelial-like):高表达TUBA1A、ACTG1,强投射到发育中人脑的神经上皮干细胞 5. 放射状胶质样(Radial glial-like):高表达LRIG1、DCLK1 6. 胚胎-神经元样(Embryonic-neuronal-like):高表达RBFOX1、CNTNAP2,富集不成熟神经元基因 7. 神经元样(Neuronal-like):高表达KIRREL3、NRXN3,富集神经元分化相关基因 8. 室管膜样(Ependymal-like):高表达DNAH9、DNAH6,富集纤毛相关基因
亚型间细胞状态组成的关键差异:
- ZFTA-RELA肿瘤主要由神经上皮样、神经元样和室管膜样细胞组成,存在向神经元和室管膜两个方向分化的连续谱
- ZFTA cluster 3肿瘤显著不同,主要由胚胎样和胚胎-神经元样细胞组成——这与其未分化的组织学表型一致
- ST-YAP1肿瘤主要展现室管膜样特征,几乎没有祖细胞存在
- 神经上皮样和胚胎样两种祖细胞样状态呈互斥分布:当神经上皮样细胞丰富时,胚胎样细胞缺失,反之亦然
尤其值得注意的是,尽管ZFTA-RELA和ZFTA cluster 3都携带相同的ZFTA-RELA融合基因,但它们的细胞状态组成截然不同。这表明融合基因类型并非决定细胞状态组成的唯一因素,发育来源和表观遗传背景同样关键。
3.3 10x Xenium空间转录组揭示ZFTA-RELA的全局空间组织模式
为了解析肿瘤细胞状态的空间分布规律,研究者对ZFTA-RELA亚型进行了大规模的10x Xenium空间转录组分析(56个切片,每个切片平均105,643个细胞,使用358个靶基因panel)。
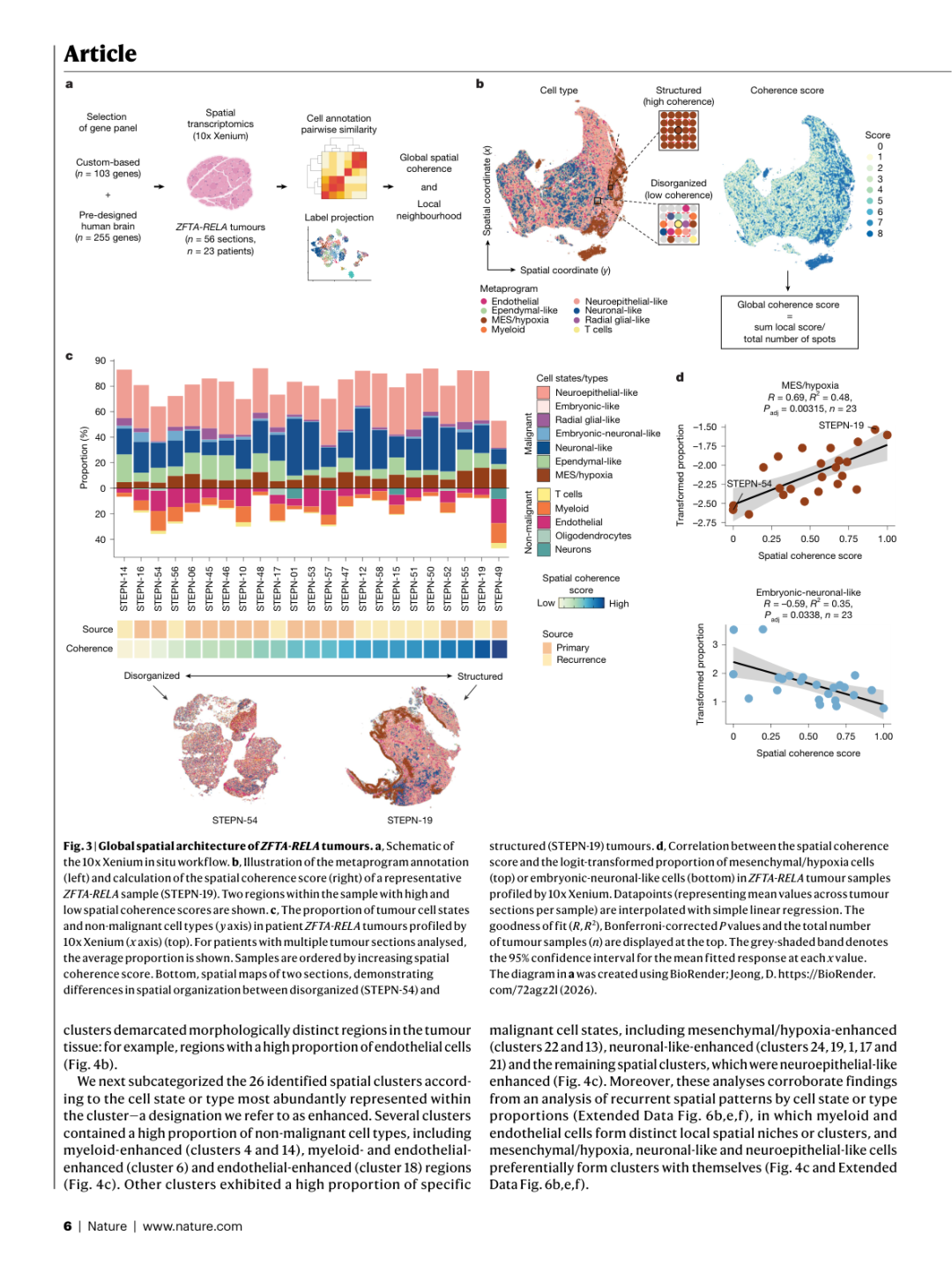
Figure 3: ZFTA-RELA肿瘤的全局空间架构
Figure 3: ZFTA-RELA肿瘤的全局空间架构
▲ Figure 3 | ZFTA-RELA肿瘤的全局空间组织模式。 (a) 10x Xenium工作流程示意图;(b) 代表性样本的元程序标注和空间一致性评分计算;(c) 所有ZFTA-RELA样本的细胞状态比例和空间组织模式,展示"结构化"与"混乱"两种类型;(d) 空间一致性评分与MES/hypoxia及胚胎-神经元样细胞比例的相关性分析。
关键发现:
1. 两种全局空间组织模式:
- 结构化肿瘤(Structured):细胞状态高度区隔化,相同状态的细胞倾向于聚集在一起(如STEPN-19)
- 混乱肿瘤(Disorganized):不同细胞状态在整个组织切片中散布分布(如STEPN-54)
2. 空间组织与细胞状态的关联:研究者定义了空间一致性评分(Spatial Coherence Score)来量化肿瘤的空间组织程度,并通过线性回归分析发现:
- 间质/低氧细胞比例与高空间一致性显著正相关(R=0.69, Padj=0.00315)
- 胚胎-神经元样细胞比例与空间一致性显著负相关(R=-0.59, Padj=0.0338)
这表明低氧环境驱动了肿瘤的区隔化组织,而胚胎-神经元样细胞则倾向于在组织中散布——这一现象在成人胶质母细胞瘤中同样被描述过,提示这可能是脑肿瘤共有的空间组织机制。
3.4 CellCharter鉴定局部空间结构
在全局空间分析的基础上,研究者进一步使用CellCharter算法对56个肿瘤切片进行跨样本的局部空间模式识别,鉴定出26个稳定的空间簇(Spatial Clusters)。
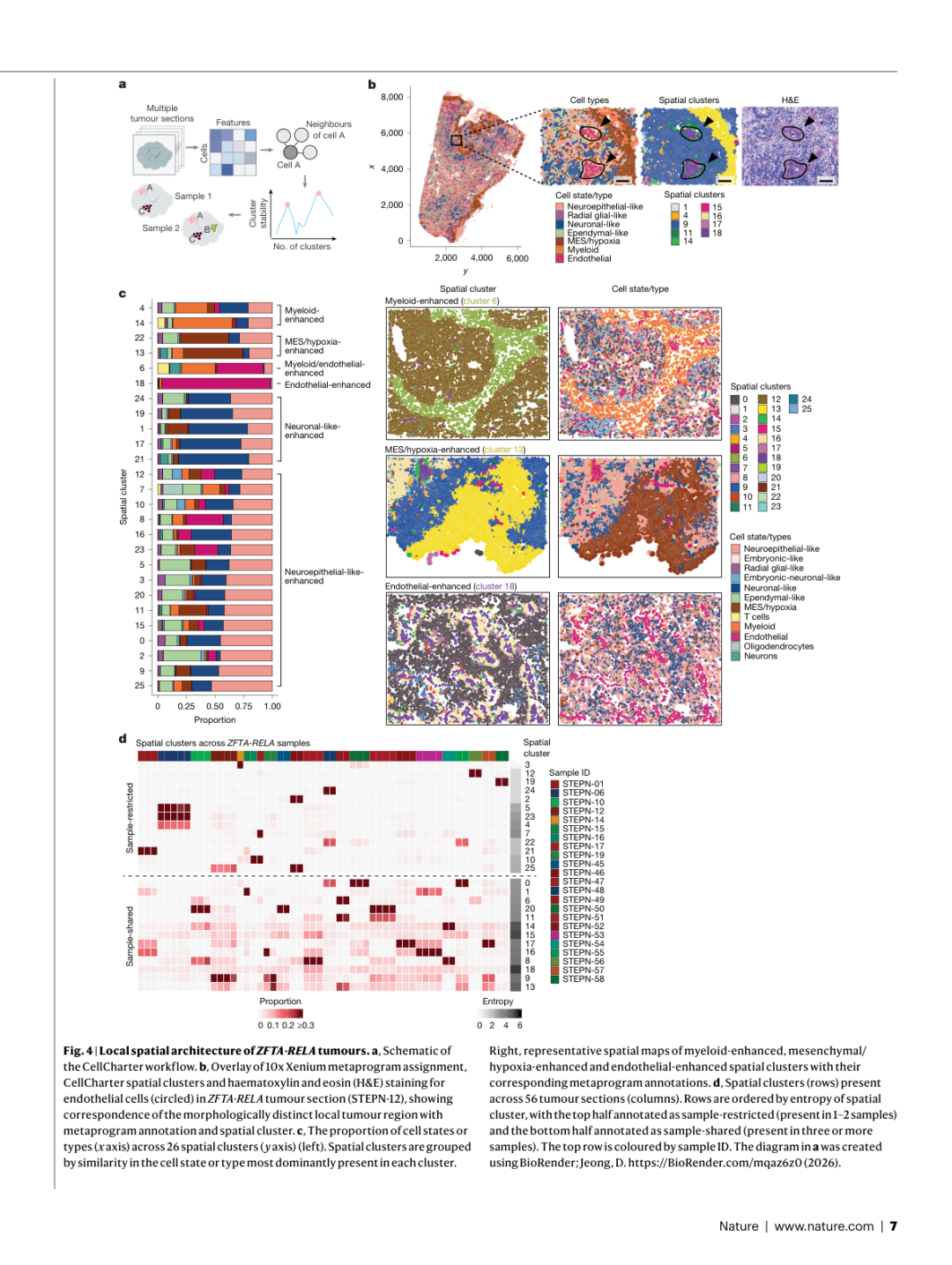
Figure 4: ZFTA-RELA肿瘤的局部空间架构
Figure 4: ZFTA-RELA肿瘤的局部空间架构
▲ Figure 4 | ZFTA-RELA肿瘤的局部空间架构。 (a) CellCharter工作流程;(b) Xenium元程序标注、CellCharter空间簇和H&E染色的叠加展示;(c) 26个空间簇的细胞状态/类型组成及代表性空间地图;(d) 空间簇在56个肿瘤切片中的分布,区分样本限制性和样本共享性簇。
核心结果:
- 26个空间簇按主导细胞状态分为多个类别:髓系增强型、内皮增强型、MES/hypoxia增强型、神经元样增强型和神经上皮样增强型
- CellCharter空间簇与H&E组织形态学特征高度对应——例如内皮增强区域与血管形态一致,室管膜细胞富集区域与室管膜玫瑰花结(ependymal rosettes)结构对应
- 空间簇可分为样本限制性(仅存在于1-2个样本)和样本共享性(存在于3个或更多样本),其中非恶性微环境细胞(髓系、内皮)形成的空间簇更倾向于跨样本共享
这些发现揭示了ST-EPNs不仅在细胞状态组成上具有异质性,在空间排列模式上同样高度多样化。MES/hypoxia、神经上皮样和神经元样细胞倾向于与自身共定位,形成状态特异性的微域结构。
3.5 脑微环境驱动细胞可塑性与形态-分子分型
研究的第三个维度关注的是肿瘤细胞在其天然神经胶质微环境中的形态学和行为学特征。
首先,研究者比较了4种体外/体内模型(单层培养、球状培养、共培养、PDX)中细胞状态的异质性:
- 单层/球状培养:主要为神经上皮样细胞(缺乏成熟细胞状态)
- 与大鼠E19皮质细胞共培养:显著增加了神经元样细胞的比例
- PDX模型:最忠实地再现了患者肿瘤的细胞状态多样性
这一发现的核心意义在于:脑驻留细胞(神经元+胶质细胞)是驱动肿瘤细胞从祖细胞状态向成熟状态可塑性转变的必要条件。
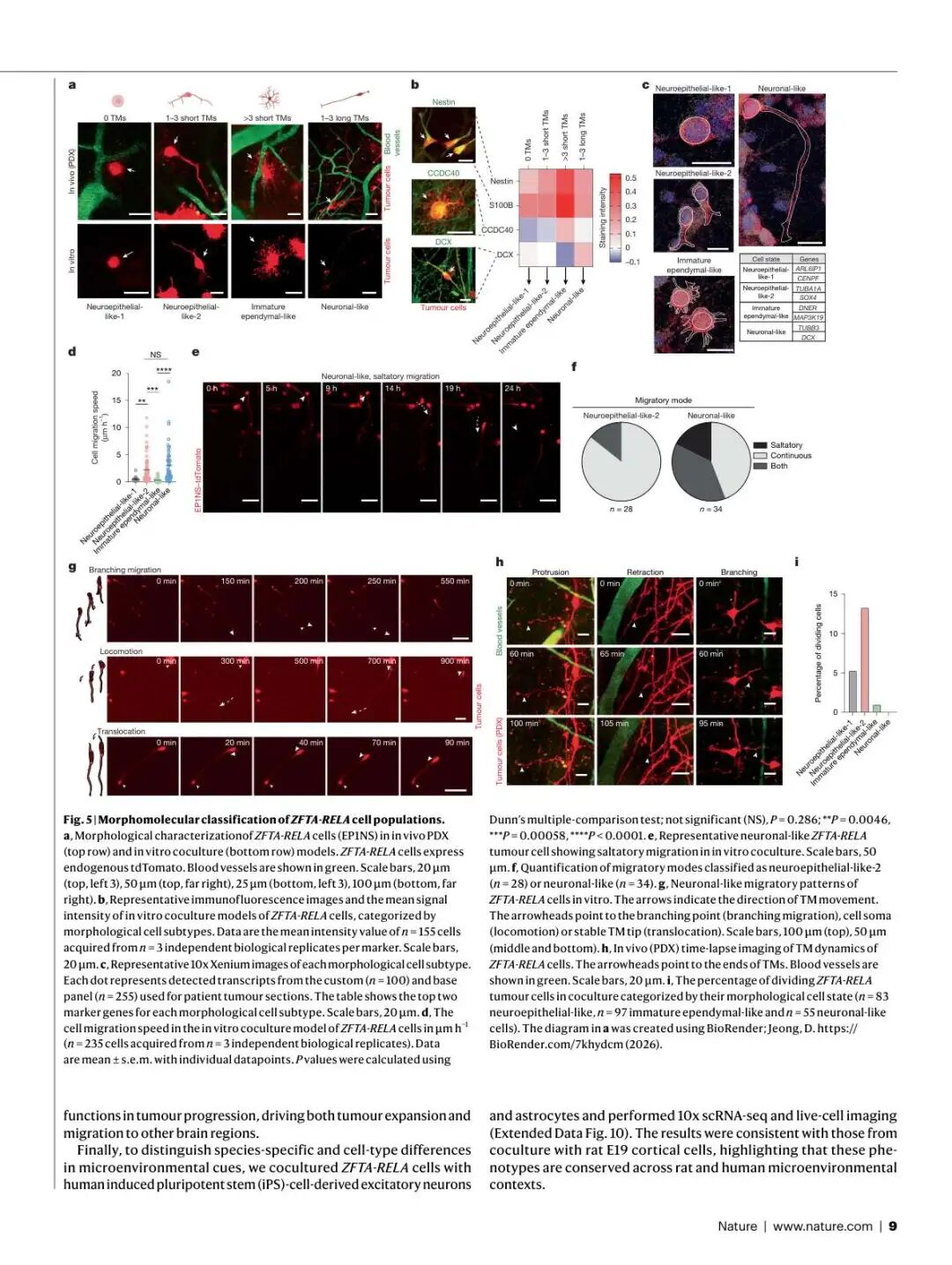
Figure 5: ZFTA-RELA细胞群的形态-分子分类
Figure 5: ZFTA-RELA细胞群的形态-分子分类
▲ Figure 5 | ZFTA-RELA细胞群的形态-分子分类与行为特征。 (a) 体内PDX和体外共培养中四种形态亚型的表征;(b) 免疫荧光验证形态与分子状态的对应关系;(c) 10x Xenium验证各形态亚型的转录特征;(d) 细胞迁移速度定量;(e) 神经元样细胞的跳跃式迁移;(f) 迁移模式分类;(g) 三种神经样迁移模式;(h) 体内肿瘤微管动力学;(i) 各细胞状态的增殖能力。
形态-分子分类体系:
研究者通过结合形态学(肿瘤微管/TMs数量和长度)和免疫荧光/Xenium分子特征,建立了四种形态-分子亚型:
形态亚型 | TM特征 | 分子标志 | 行为表型 |
|---|---|---|---|
神经上皮样-1 | 无TM (0 TMs) | ARL6IP1+, CENPF+ | 静止型,中等增殖 |
神经上皮样-2 | 1-3个短TM | TUBA1A+, NES+, DCX+ | 高迁移+高增殖(双能力) |
不成熟室管膜样 | >3个短TM | MAP3K19+, CCDC40+ | 静止型 |
神经元样 | 1-3个长TM (>100μm) | TUBB3+, DCX+ | 高迁移(跳跃式) |
迁移行为的关键发现:
- 神经元样细胞和神经上皮样-2细胞是最具迁移能力的群体
- 两者采用不同的迁移模式:
- 神经上皮样-2细胞:多采用连续迁移模式
- 神经元样细胞:更常采用跳跃式迁移模式(saltatory migration)——这是发育过程中未成熟神经元的典型迁移方式
- 神经元样细胞展示了三种类神经迁移模式:分支迁移(branching migration)、运动(locomotion)和转位(translocation)
- 肿瘤微管展现出类似发育中神经突起的动态行为:伸出(protrusion)、回缩(retraction)和分支(branching)
最具临床警示意义的发现:神经上皮样-2细胞同时具备高迁移能力和高增殖能力。这种"双能力"群体可能在肿瘤进展中发挥关键作用——既能驱动肿瘤扩张,又能向其他脑区迁移。这对室管膜瘤的复发和远处转移具有重要提示意义。
四、讨论与临床意义
4.1 发育起源与治疗策略
本研究揭示了不同ST-EPN亚型具有截然不同的发育特征和分化谱系。这些差异性特征为个性化治疗策略的开发奠定了基础。特别是:
- ZFTA cluster 3的胚胎样特征提示可能需要针对早期发育通路的靶向策略
- ST-YAP1的室管膜样特征提示其可能对分化诱导治疗更为敏感
- ZFTA-RELA的双向分化特征(神经元+室管膜)增加了治疗的复杂性
4.2 低氧与空间组织
低氧作为全局空间结构化的驱动因素,在成人胶质瘤中也已被报道,提示这是脑肿瘤共有的组织学特征。低氧在后颅窝室管膜瘤中已被证实对代谢和表观遗传调控至关重要,但其在幕上室管膜瘤中的作用此前被低估。
4.3 迁移亚群的临床意义
神经元样细胞利用神经发育中的迁移机制(如跳跃式迁移、微管动力学)在脑实质中侵袭——这一特征在胶质母细胞瘤中也被观察到。对于室管膜瘤而言,这一发现尤为重要:室管膜瘤通常被认为最初主要以局部生长为主,仅在复发时才出现远处转移。本研究提示,在手术切缘处检测迁移性肿瘤亚群可能对预后评估具有价值。
五、技术方法学亮点
本研究在方法学层面同样具有重要参考价值:
- Xenium面板设计策略:结合自定义面板(源自sc/snRNA-seq的标志基因)和预设面板(人脑细胞类型基因),并创新性地加入融合基因特异性探针——这为其他融合基因驱动肿瘤的空间分析提供了范式
- 空间一致性评分:自主开发的空间组织量化指标,通过将组织切片网格化并计算相邻区域的细胞状态一致性来定量全局空间结构
- CellCharter跨样本空间分析:同时对56个切片进行局部空间模式识别,利用变分自编码器进行降维和批次校正
- 形态-分子整合分类:通过免疫荧光+Xenium+活细胞成像三重验证,建立了细胞形态与转录状态的精确对应关系
六、总结与展望
本研究通过整合单细胞/单核转录组学、10x Xenium亚细胞分辨率空间转录组学以及体内/体外活细胞成像,构建了ST-EPN肿瘤异质性的多维度分析框架。研究的核心贡献可以归纳为以下几点:
未来方向:
- 需要大规模临床队列来比较所有分子亚型的患者预后和治疗抵抗差异
- 需要在ST-EPN模型中直接研究低氧驱动的组织结构变化及其功能意义
- 需要在手术切缘组织中检测迁移性肿瘤亚群,评估其对肿瘤侵袭和复发的贡献
- 神经上皮样-2细胞的双能力(迁移+增殖)使其成为潜在的治疗靶标
本研究不仅为ST-EPN提供了前所未有的细胞状态和空间图谱,更重要的是建立了一个可推广的方法学框架——整合转录组学、空间组学和功能表型分析,对其他类型脑肿瘤乃至实体瘤的异质性研究具有广泛的借鉴意义。
参考文献:Jeong D, Danielli SG, et al. Multidimensional profiling of heterogeneity in supratentorial ependymomas. Nature (2026). DOI: 10.1038/s41586-026-10214-2 IF: 48.5 Q1 B1
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-08,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

