第20篇HD文章(正刊)--癌症中异位表达的NMDAR揭示了种系编码的自身免疫性
原创第20篇HD文章(正刊)--癌症中异位表达的NMDAR揭示了种系编码的自身免疫性
原创
追风少年i
发布于 2026-03-30 10:11:17
发布于 2026-03-30 10:11:17
作者,Evil Genius
无论发生什么,生活都要继续。
现在的文章,多多少少都有点结构生物学的影子,看来文章真的是不仅仅要求发现问题,还要为解决问题提供一个可能的思路。
今天我们分享HD文献,这些正刊真是的话虽然不多,信息密度真的大。

知识积累
适应性免疫系统在进化过程中形成了区分自我与非我的能力。
副肿瘤性自身抗体可调节宿主(例如改变神经元功能)和肿瘤(例如抑制肿瘤生长和转移)。事实上,在自身免疫发生后甚至观察到过肿瘤自发消退的现象。目前公认抗体介导和T细胞介导的免疫协同作用共同驱动肿瘤的免疫控制。激活T细胞介导免疫的疗法可能诱发显著的抗体介导神经元自身免疫,且这种自身免疫与抗肿瘤疗效的改善相关。
异位表达的癌神经抗原可募集种系构型B细胞,这些B细胞在三级淋巴结构中经历亲和力成熟,产生能穿过血脑屏障的髙亲和力IgG自身抗体。
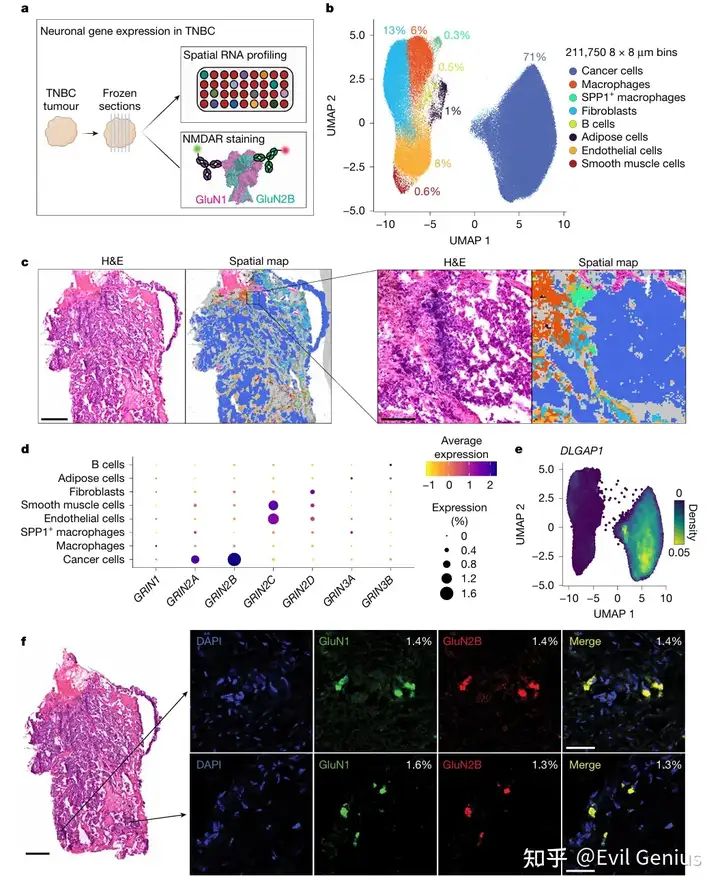
结果1、TNBC中GluN1–GluN2B的表达
通过对METABRIC和TCGA数据库(bulk)的再分析,研究确认部分乳腺癌同时表达GRIN1和GRIN2B,其中GRIN1在雌激素受体阳性肿瘤中高表达,而GRIN2B在TNBC中显著富集。进一步对TNBC切片进行空间RNA(visium HD)分析发现,GRIN2B转录本仅存在于癌细胞cluster中,且癌细胞也表达NMDAR支架蛋白GKAP。免疫荧光分析最终在1-2%的肿瘤细胞中验证了GluN1和GluN2B蛋白的表达。
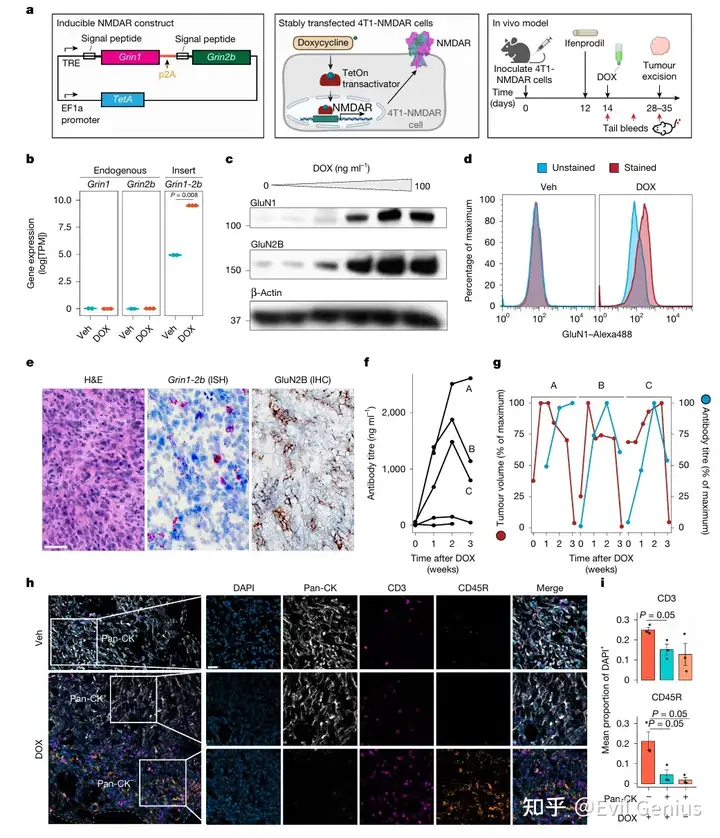
结果2、NMDAR诱导的B细胞反应
NMDAR表达是肿瘤进展过程中出现的新特征。
通过建立多西环素诱导表达GluN1-GluN2B的4T1小鼠三阴性乳腺癌模型,发现癌细胞中异位表达的NMDAR亚基(GRIN1和GRIN2B)具有高度免疫原性。单细胞RNA测序显示,高表达Grin1-2b的癌细胞cluster增殖标志物上调,同时肿瘤浸润中性粒细胞表达xCT,可能参与旁分泌信号。诱导NMDAR表达后,小鼠体内抗NMDAR抗体滴度在两周内达峰,高滴度个体出现肿瘤自发消退;肿瘤组织表现为B细胞、T细胞和巨噬细胞富集,并形成三级淋巴结构。这些结果表明,肿瘤细胞中异位表达的NMDAR足以诱导强大的适应性免疫应答,尤其是抗NMDAR体液免疫。
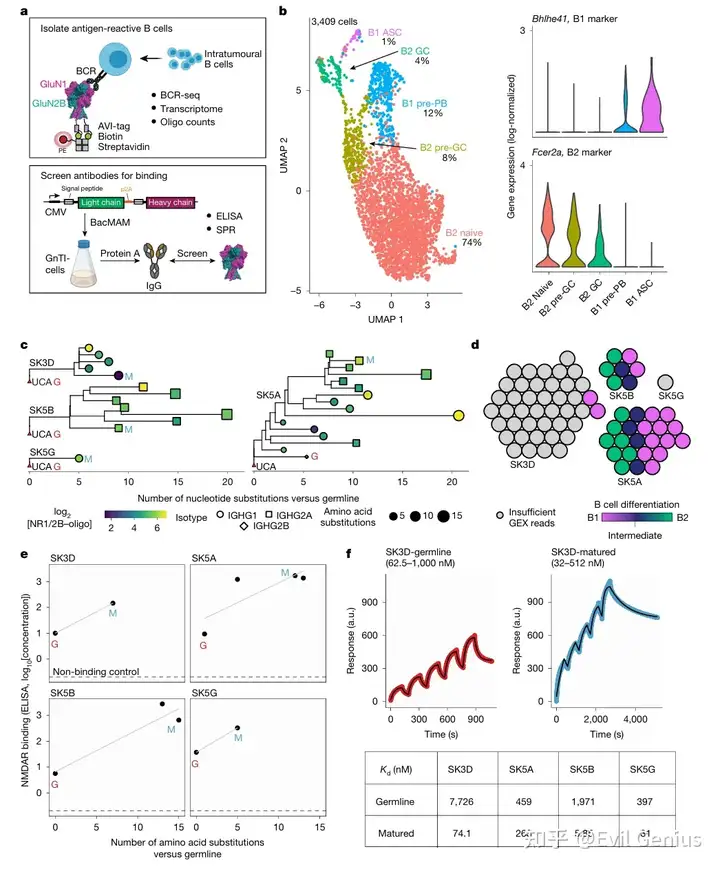
结果3、种系抗体保留NMDAR结合能力
研究通过对4T1-NMDAR肿瘤模型中NMDAR结合B细胞的分析,揭示了抗NMDAR抗体起源于种系构型幼稚B细胞。研究人员从抗体滴度升高的小鼠肿瘤内分选并测序了3,180个NMDAR结合B细胞,鉴定出从幼稚到抗体分泌细胞的一系列分化状态,其中所有前浆母细胞和抗体分泌细胞均表现为Bhlhe41高表达和Fcer2a低表达。通过构建BCR系统发育树,筛选出四个具有NMDAR结合能力的克隆型,每个克隆型均包含种系序列和经过体细胞高频突变的成熟序列,其中SK5A克隆型发生了多达四次的类别转换事件。重组表达和ELISA实验证实,所有四个克隆型的种系抗体和成熟抗体均能特异性结合GluN1-GluN2B,而不结合BSA或多反应性抗体常见靶标。表面等离子体共振(SPR)分析进一步显示,种系抗体对NMDAR的结合亲和力较低(Kd范围为397–7,726 nM),而成熟抗体的亲和力显著提高(Kd范围为5.85–263 nM),证实了亲和力成熟过程。此外,对肿瘤引流淋巴结来源B细胞的分析发现,具有NMDAR结合能力的细胞主要是未突变的幼稚B细胞,且从中筛选出两种未突变抗体同样具有NMDAR结合能力。这些结果共同证明,NMDAR反应性B细胞来源于天然存在的种系构型幼稚B细胞,这些细胞在肿瘤内经历体细胞高频突变和类别转换后,发育为高亲和力的成熟抗体。
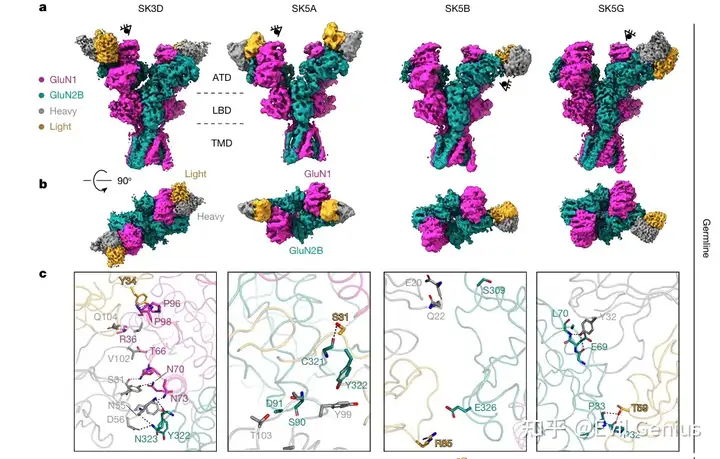
结果4、冷冻电镜揭示表位汇聚
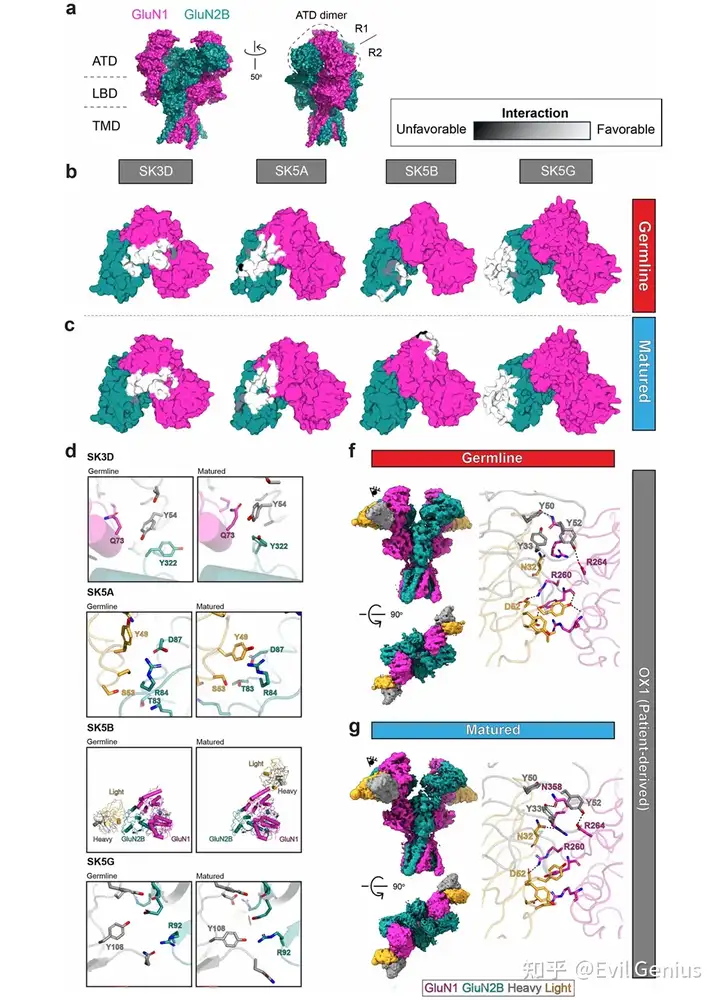
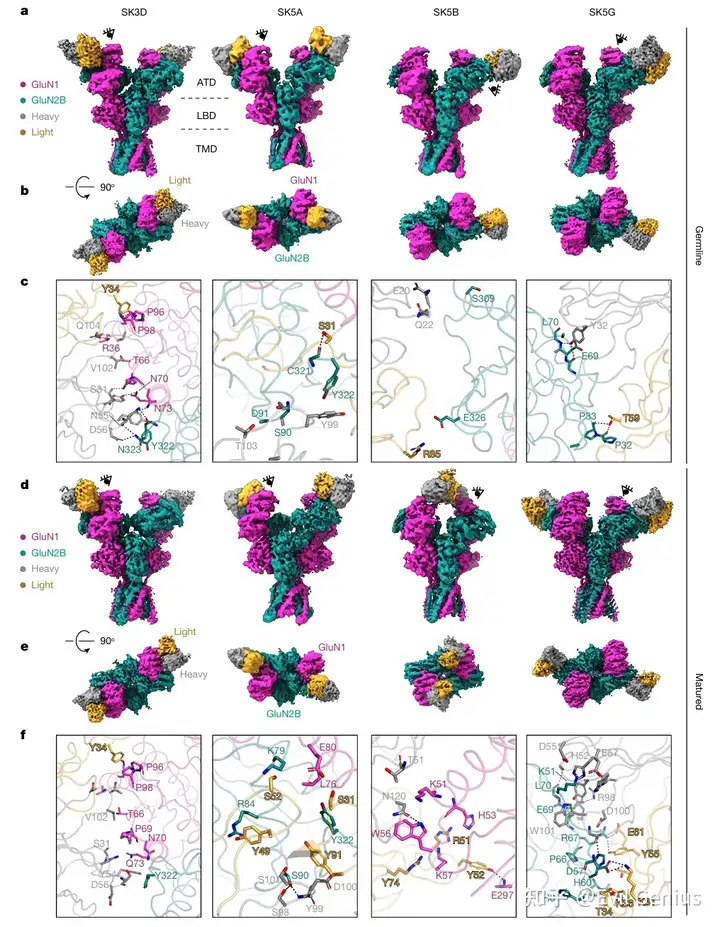
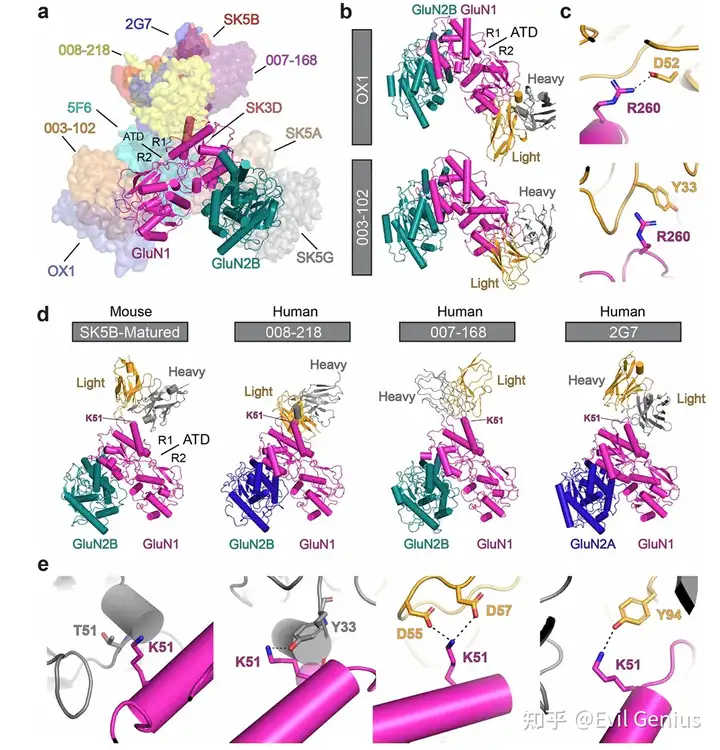
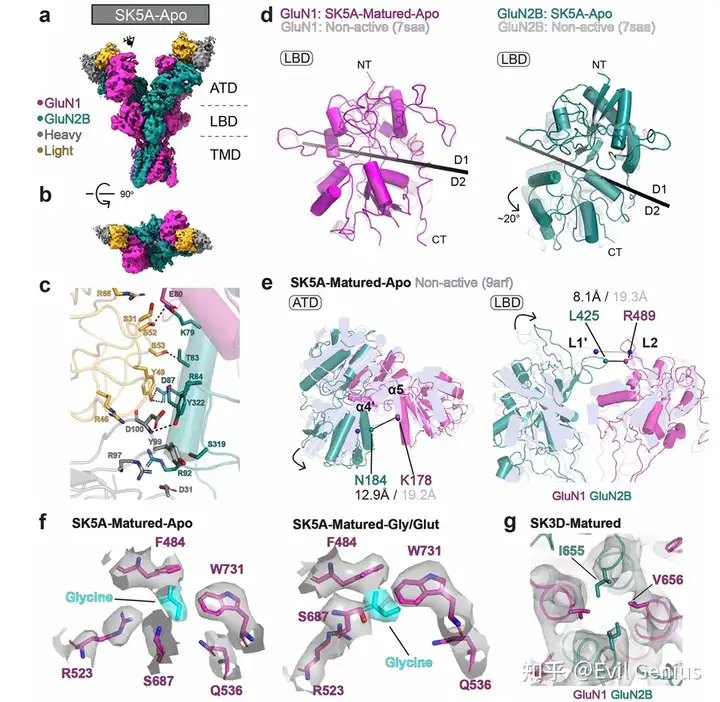
为了探究肿瘤来源的抗NMDAR抗体的表位特征,对四个小鼠肿瘤来源克隆型的代表性种系抗体和成熟抗体与GluN1-GluN2B复合物进行了冷冻电镜结构解析。所有抗体均结合于NMDAR的氨基末端结构域(ATD),表位均匀分布于GluN1和GluN2B亚基之间。其中SK3D和SK5A两种成熟抗体结合于GluN1-GluN2B ATD R1叶的界面区域。结构分析显示,亲和力成熟伴随着抗体-抗原相互作用的增强:在SK3D克隆型中,成熟抗体通过GluN1 Gln73、GluN2B Tyr322与重链CDR2区域Tyr54的协同配位实现亲和力提升;在SK5B克隆型中,种系抗体仅与GluN2B ATD R1叶存在微弱静电相互作用,而成熟抗体则转向结合GluN1 ATD的氨基末端,发生了表位扩散现象;在SK5G克隆型中,成熟抗体通过重链CDR3区域Tyr108与GluN2B Arg92的增强配位提高了亲和力。此外,研究者还从ANRE患者OX1中分离出相关IgG1 B细胞,其成熟抗体(OX1-matured)的Fab片段与NMDAR结合的Kd为83.7 nM,冷冻电镜分析显示OX1成熟抗体和种系抗体均结合于GluN1 ATD的R2叶重叠表位。通过与已报道的患者来源抗体结构比较,发现多个抗体表位存在明显收敛:OX1与003-102抗体均与GluN1 Arg260形成极性相互作用;SK5B成熟抗体在GluN1 ATD R1叶的表位与008-218、007-168和2G7三种患者来源抗体直接重叠,其中高度暴露的GluN1 Lys51构成免疫优势表位的一部分;SK5A和SK3D则结合于GluN1-GluN2B亚基界面,与部分患者来源抗体选择性识别异源二聚体的特征一致。这些发现揭示了肿瘤来源抗体在克隆型内部和克隆型之间表位的多样性,并证明了跨物种的表位收敛于GluN1-GluN2B ATD区域。
结果5、抗NMDAR抗体在功能上有所不同
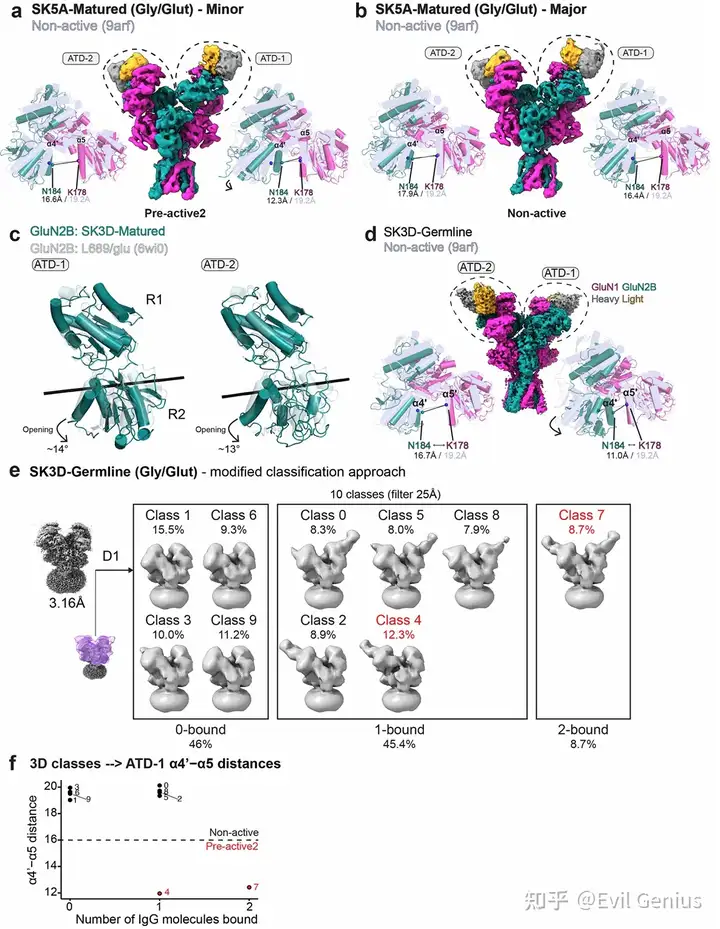
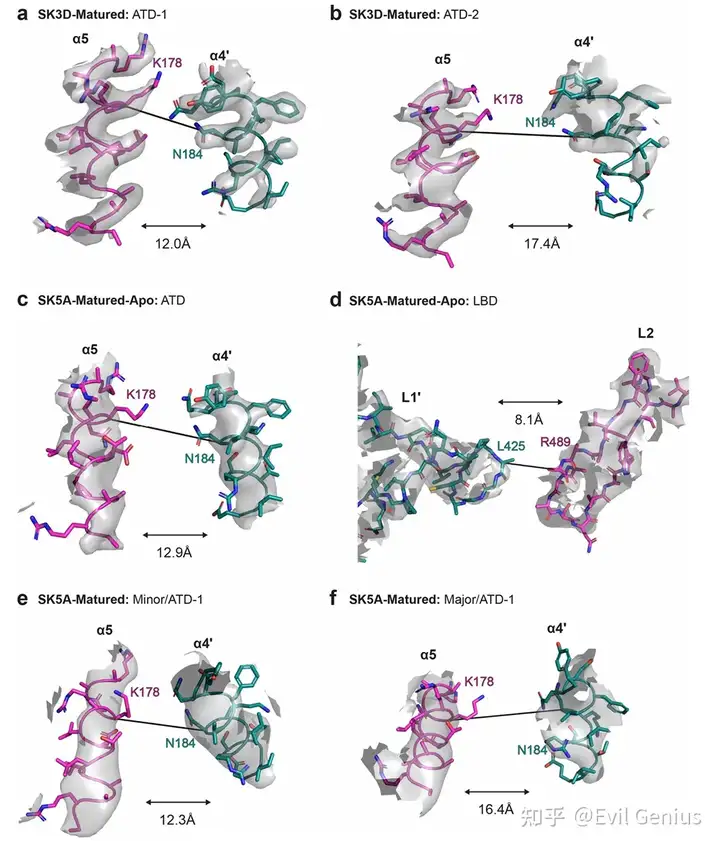
通过电生理和冷冻电镜结构分析,系统揭示了肿瘤来源的抗NMDAR抗体对通道功能的不同调节作用及其结构基础。研究者首先利用抗体结合后的NMDAR结构,测量了反映受体构象状态的关键距离参数(α4′–α5和L1′–L2),发现SK3D成熟抗体和SK5A成熟抗体结合的受体呈现一种此前未被报道的构象状态(命名为pre-active2),其特征是仅ATD-1异源二聚体中的α4′–α5距离缩短,而LBD区域的L1′–L2距离保持不变。进一步分析显示,SK3D种系抗体结合的受体中仅约21%呈现pre-active2构象,而成熟抗体结合后该构象比例显著增加,表明亲和力成熟与受体调节能力相关。SK5A成熟抗体的结合不依赖激动剂,在无甘氨酸和谷氨酸条件下仍能结合相同的表位残基,并稳定受体于gly/apo状态。通过对所有抗体-NMDAR复合物的构象进行分类,研究者将受体状态分为gly/apo、pre-active、open、pre-active2和non-active五种类型。基于构象特征,研究者准确预测了各抗体的功能效应:SK3D成熟抗体和SK5A成熟抗体呈剂量依赖性增强NMDAR通道电流(333 nM时增强超过200%),SK5G成熟抗体则抑制通道活性,而SK5B成熟抗体仅有微弱增强作用(333 nM时小于20%),非结合对照抗体无任何效应。在体外细胞毒性实验中,具有通道增强作用的SK3D抗体表现出剂量依赖的细胞毒性(IC50为120 nM),而抑制性抗体SK5G则具有保护作用。在B细胞缺陷小鼠的4T1-NMDAR肿瘤模型中,SK3D抗体治疗显著增强了肿瘤消退,其中2/4的肿瘤达到接近完全病理缓解,肿瘤组织中上皮特异性转录本几乎检测不到,而免疫相关转录本显著富集。重要的是,抗体对通道电流的功能调节效应与α4′–α5距离呈高度相关(r²=0.98,P=0.0059),证实冷冻电镜结构分析对预测自身抗体功能效应具有直接指导意义。这些结果共同表明,肿瘤来源的抗NMDAR抗体可产生从强抑制到强增强的完整功能调节谱系,其效应可通过结构分析准确预测。
结果6、抗体转移重现了ANRE
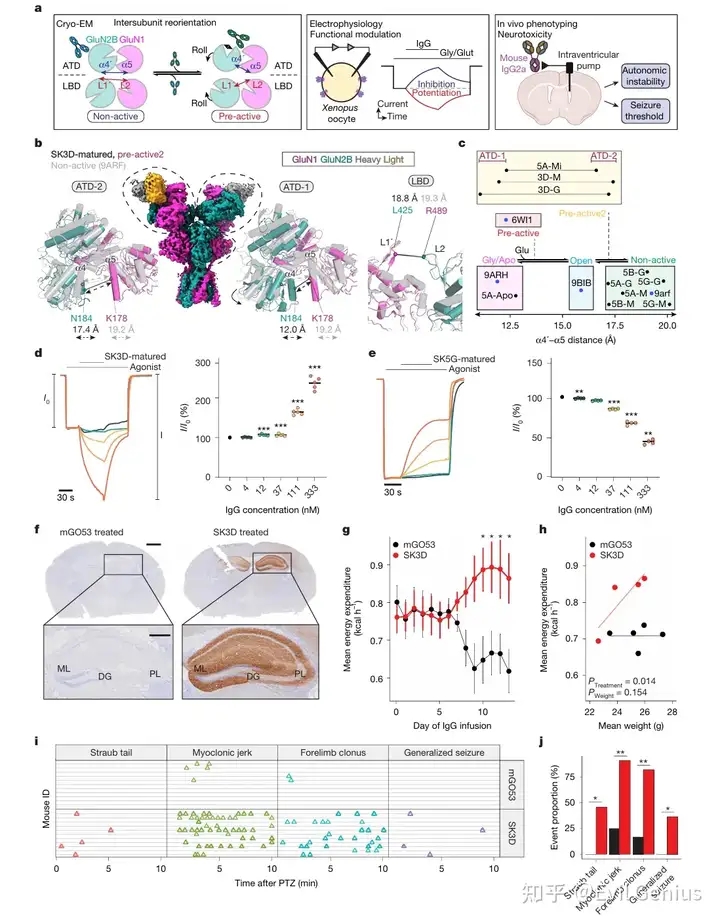
研究通过被动转移实验,直接验证了肿瘤来源的NMDAR调节性抗体足以引发ANRE的典型症状。研究者通过脑室内植入微量泵,向健康雌性小鼠持续输注抗体(40 μg/天,持续14天),以排除肿瘤系统性影响。实验重点检测了ANRE最核心的两个临床表现:自主神经功能障碍(主要表现为高热)和癫痫发作阈值降低。
结果显示,输注通道增强型抗体SK3D成熟抗体的小鼠,从第7天开始总能量消耗显著增加(第10天达统计学显著),且这种增加与体重和活动量无关,最可能反映产热增加导致的体温升高。在暗周期(小鼠活跃期)观察到明显的高热现象。相比之下,输注通道抑制型抗体SK5G成熟抗体的小鼠则表现为运动活性显著增强,这与NMDAR通道抑制剂的已知效应一致。
在癫痫发作阈值实验中,研究人员给予亚惊厥剂量的戊四氮(GABA受体拮抗剂,20 mg/kg)后发现,SK3D处理组小鼠在注射后10分钟内,尾部背屈、肌阵挛性抽搐、前肢阵挛和全身强直-阵挛发作四种典型癫痫事件的发生率和复发频率均显著高于对照组。所有SK3D处理小鼠均表现出癫痫活动,其中4只发展为全身性发作。而SK5G处理组未观察到显著的癫痫活动。通过海马区抗Flag染色证实了SK3D抗体的靶向递送。
这些结果表明,SK3D成熟抗体(其种系构型B细胞受体保留NMDAR结合能力)的脑室内输注,足以复制ANRE患者常见的自主神经调节障碍和癫痫发作阈值降低两大核心特征,而通道抑制型抗体SK5G则不产生这些表型。这直接证明了种系编码抗体与ANRE发病之间的因果关系。
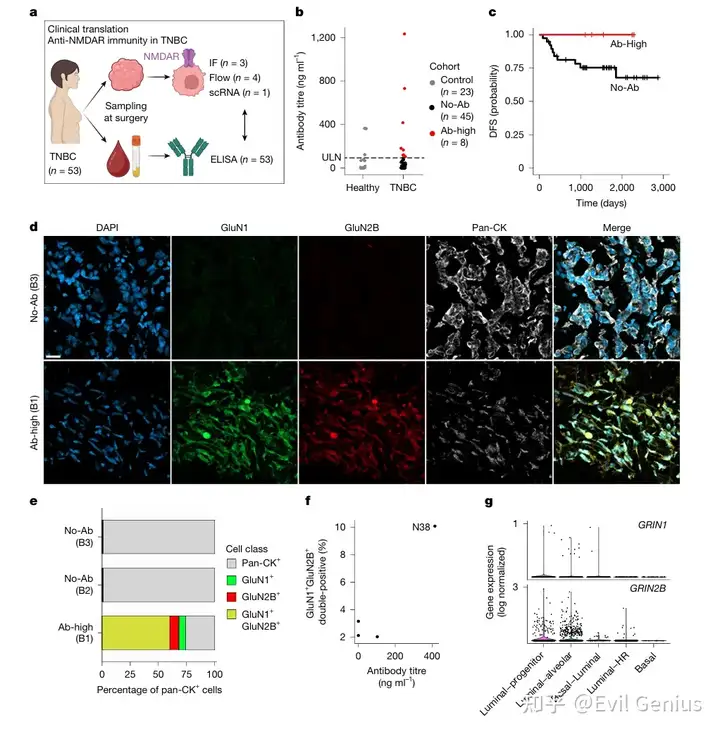
结果7、人类TNBC中的抗NMDAR抗体
分析了53例三阴性乳腺癌(TNBC)患者的血浆样本,发现其中8例(15%)患者的抗NMDAR抗体滴度超过正常值上限(95%置信区间)。在中位4.29年的随访期内,这些抗体高滴度患者均未出现疾病进展。通过免疫荧光和流式细胞术检测,在抗体高滴度患者的肿瘤组织中可检测到上皮来源的GluN1-GluN2B表达,而抗体阴性患者则未检测到。流式细胞术进一步显示,不同患者的GluN1-GluN2B双阳性细胞比例存在差异,其中抗体滴度最高的患者(N38,滴度416 ng/ml)呈现最高的阳性细胞比例。对该患者肿瘤组织的单细胞RNA测序分析显示,GRIN1和GRIN2B主要表达于缺乏ESR1表达的管腔祖细胞样(KIT+KRT23+)和管腔肺泡样(ELF5+)癌细胞亚群;同时在T细胞组分中观察到与三级淋巴结构形成及良好预后相关的细胞毒性CD8+ T细胞和滤泡辅助性T细胞样CD4+ T细胞(CXCL13+IGFL2+)。这些结果揭示了肿瘤内源性NMDAR表达与循环抗NMDAR抗体之间的强相关性,支持抗NMDAR免疫应答抑制TNBC肿瘤生长的模型。
生活很好,有你更好
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

