文献分享--单细胞图谱描绘化疗后肝母细胞瘤的免疫细胞重塑与增强的肿瘤-成纤维细胞相互作用
原创文献分享--单细胞图谱描绘化疗后肝母细胞瘤的免疫细胞重塑与增强的肿瘤-成纤维细胞相互作用
原创
追风少年i
发布于 2026-03-30 16:08:30
发布于 2026-03-30 16:08:30
作者,Evil Genius
事业编考试马上就要开始了,大家准备好了么?只要有破釜沉舟的勇气,就一定能考上。
大家最近都在OpenClaw,而对于组学分析呢,基本上也有了omicsclaw,基本上代码部分省了很多事情,我们只需要理解关键的参数部分即可,然后文字书写分析需求,写上参数即可。
不过想要构建思路,灵活运用代码,做一些个性化的分析,目前还需要人工来做,以后工作两级分化了,光会使用属于初级,有工作的必须在AI的基础上进一步提升。
今天我们分享文献
知识积累
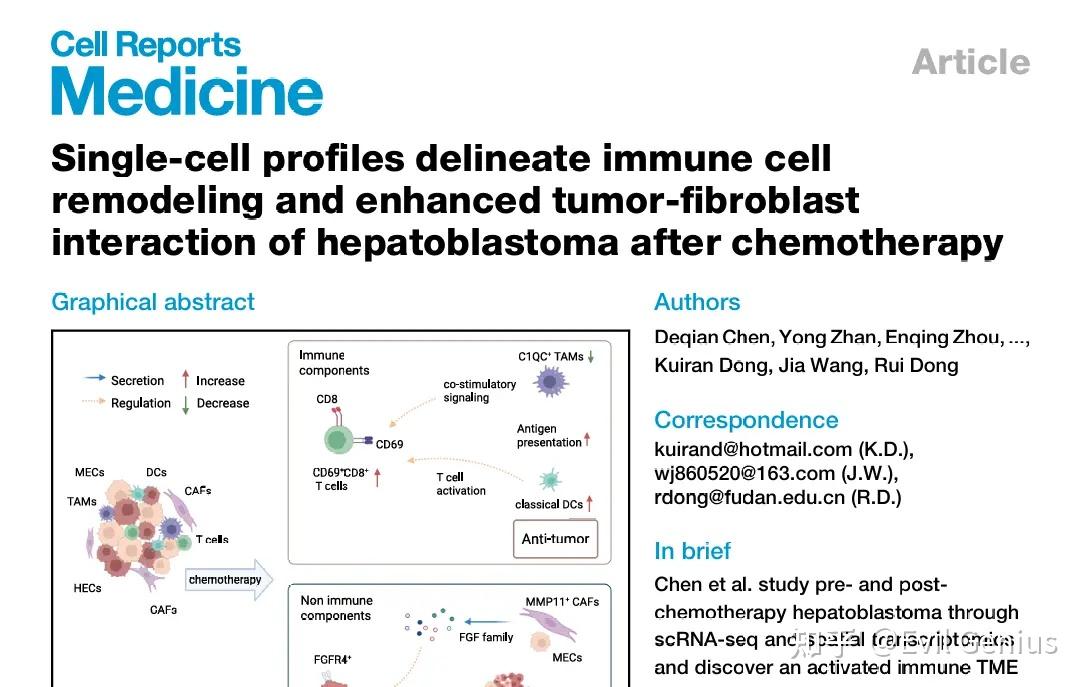
肝母细胞瘤(HB)
定义:一种罕见的婴幼儿肝脏恶性肿瘤,发病率近三十年显著上升。
起源:被认为起源于肝脏前体细胞(肝母细胞)。
病理特征:通常在同一肿瘤内混合存在胎儿型、胚胎型和间质型三种组织学类型。
遗传驱动:主要遗传驱动因素是CTNNB1基因的变异。
免疫细胞重塑:化疗会富集CD69+ CD8+ T细胞,并使髓系细胞向免疫激活表型转变。
肿瘤细胞异质性:恶性上皮细胞呈现肝细胞样和间质样表型的混合;高度增殖的肿瘤细胞主要属于肝细胞谱系,且高表达FGFR4。
基质细胞互作:发现一群MMP11+ 癌症相关成纤维细胞,在化疗后通过FGF-FGFR4信号通路与肿瘤细胞增强交互。
治疗启示:研究揭示了免疫细胞对化疗的响应,并指出FGF-FGFR信号与化疗耐药相关,提示FGFR4阻断可能具有治疗潜力。
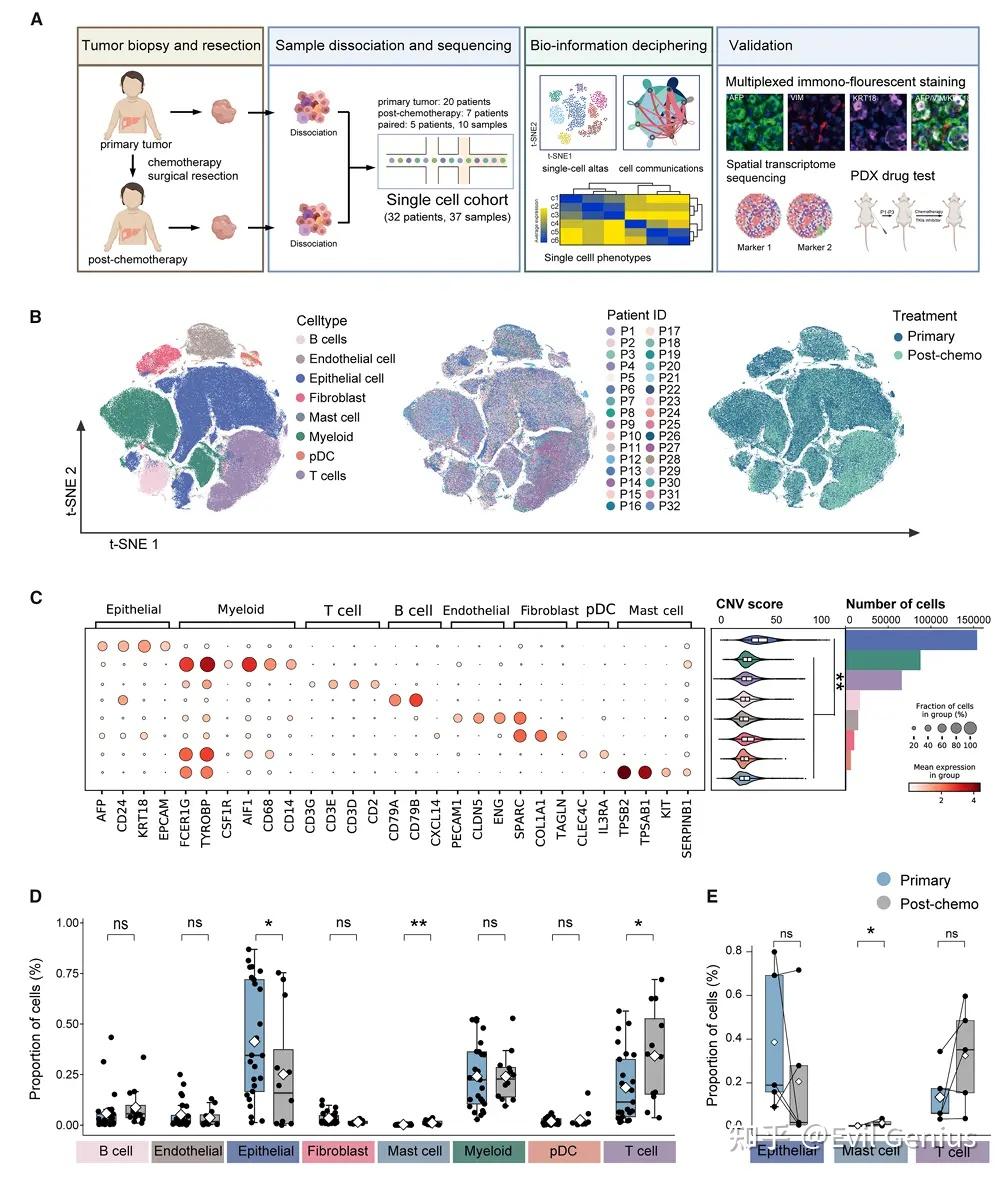
结果1、原发性和化疗处理样本中HB微环境的单细胞分类学
单细胞数据分析
主要分类:通过经典标记基因将细胞分为三大类:
上皮细胞(占69%):被鉴定为恶性肿瘤细胞(基于拷贝数变异分析)。
免疫细胞(占14%):包括T细胞、自然杀伤T细胞、巨噬细胞、浆细胞样树突状细胞和B细胞。
基质细胞(占10%):包括成纤维细胞和内皮细胞。
化疗后的关键变化
肿瘤细胞减少:化疗后,上皮(肿瘤)细胞的比例平均下降了1.5倍,证实了化疗的抗肿瘤效果(在5对配对样本中,有4例呈现下降趋势)。
T细胞浸润增加:化疗后,T细胞的比例平均增加了2.4倍,表明化疗可能促进了免疫细胞的浸润(在5对配对样本中,有4例呈现增加趋势)。
肥大细胞显著增加:在所有样本及配对样本分析中,化疗后肥大细胞的比例均显著上升。
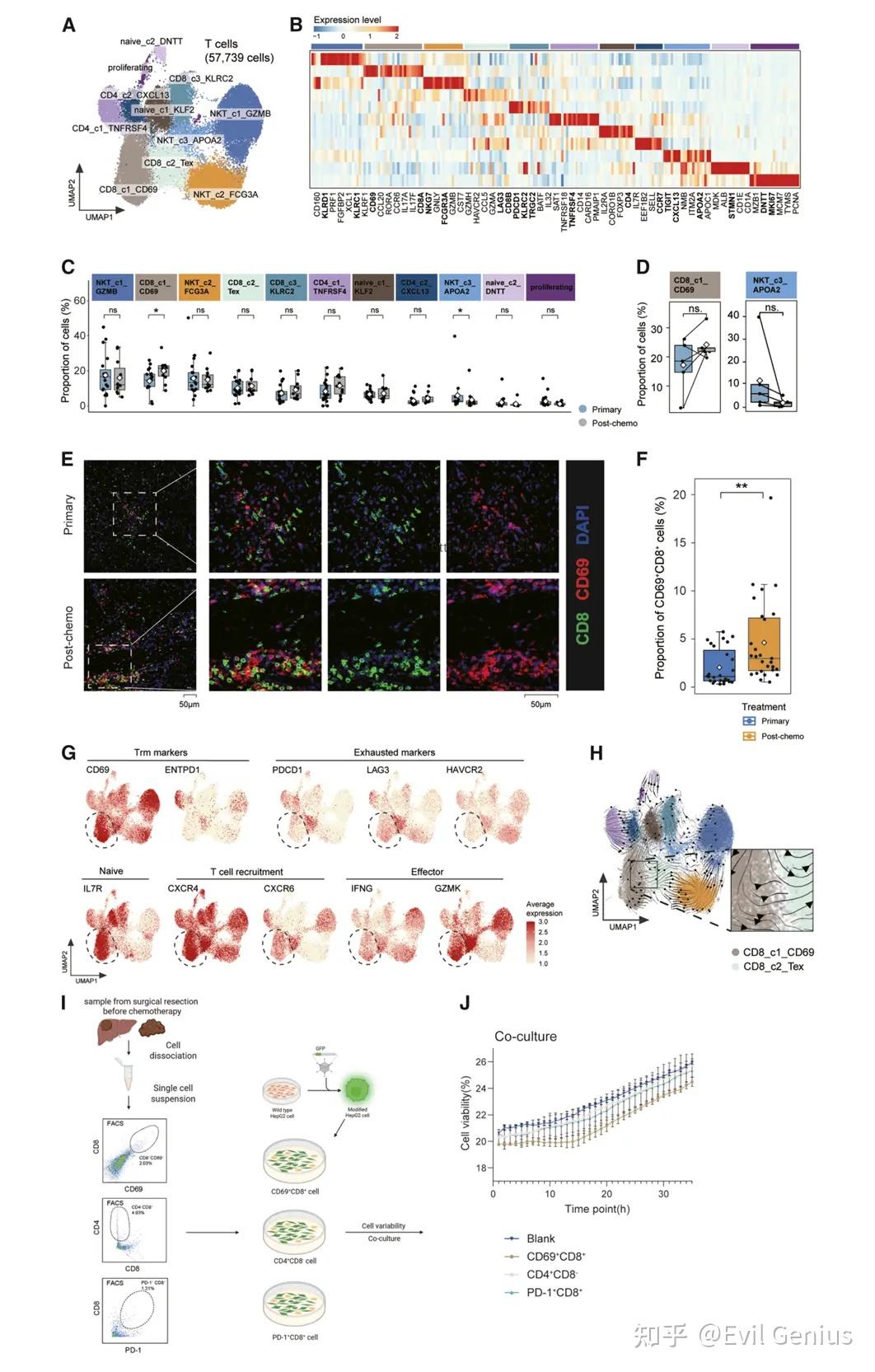
结果2、化疗后CD69+CD8+T细胞的富集
背景:基于化疗后T细胞浸润增加的现象,进一步深入分析T细胞亚群。
亚群分类:从57,739个T细胞中鉴定出11个集群,主要包括:
CD4+ Treg
CD8+ T细胞(三个主要亚群):
- CD8+_c1_CD69+:表达组织驻留标记CD69。
- CD8_c2_Tex:表达耗竭标记LAG3。
- CD8+_c3_KLRC2:表达细胞毒性标记KLRC2和TRGC2。
NKT细胞。
化疗后CD69+ CD8+ T细胞的富集与验证
富集现象:CD69+ CD8+ T细胞在化疗后显著增加(5对配对样本中有4例比例升高)。
实验验证:通过多重免疫组化染色分析9对匹配样本,进一步证实了化疗后CD69+ CD8+ T细胞水平升高。
CD69+ CD8+ T细胞的分子特征
非耗竭/非驻留表型:不表达组织驻留标记CD39,也不表达耗竭标记PDCD1、LAG3、HAVCR2。
功能相关标记:高表达T细胞募集标记(CXCR4、CXCR6)、效应分子(IFNG、GZMK)以及IL7R(提示其具有相对初始样的特征)。
分化轨迹:RNA速率分析显示,CD69+ CD8+ T细胞位于向Tex分化的上游路径,提示其可能是一种先天样状态,具有抗肿瘤免疫潜力。
细胞功能实验验证
实验设计:通过流式细胞分选技术从肿瘤样本中分选出CD69+ CD8+ T细胞、CD4+ T细胞和PD-1+ CD8+ T细胞(Tex),分别与GFP+HepG2肝癌细胞共培养,监测肿瘤细胞存活率。
实验结果:CD69+ CD8+ T细胞表现出最强的肿瘤细胞毒性效应,提示其可能是有效的抗肿瘤亚群。
化疗后T细胞的功能增强
转录动态:化疗后的CD69+ CD8+ T细胞显著上调了T细胞效应分子(GZMB、GNLY、PRF1、IFNG)和抗原呈递相关基因(HLA-DRB1、HLA-DRB5、HLA-DQA2)。
其他T细胞:Tex和NKT细胞在化疗后也表现出增强的效应功能(效应分子和HLA家族基因上调)。
耗竭标记:未发现Tex细胞中PDCD1、TIGIT等耗竭相关基因在化疗后发生显著一致性变化。
化疗可能通过两种机制在肝母细胞瘤中诱导抗肿瘤免疫反应:
富集CD69+ CD8+ 组织驻留样T细胞。
增强不同T细胞亚群的细胞毒性功能。
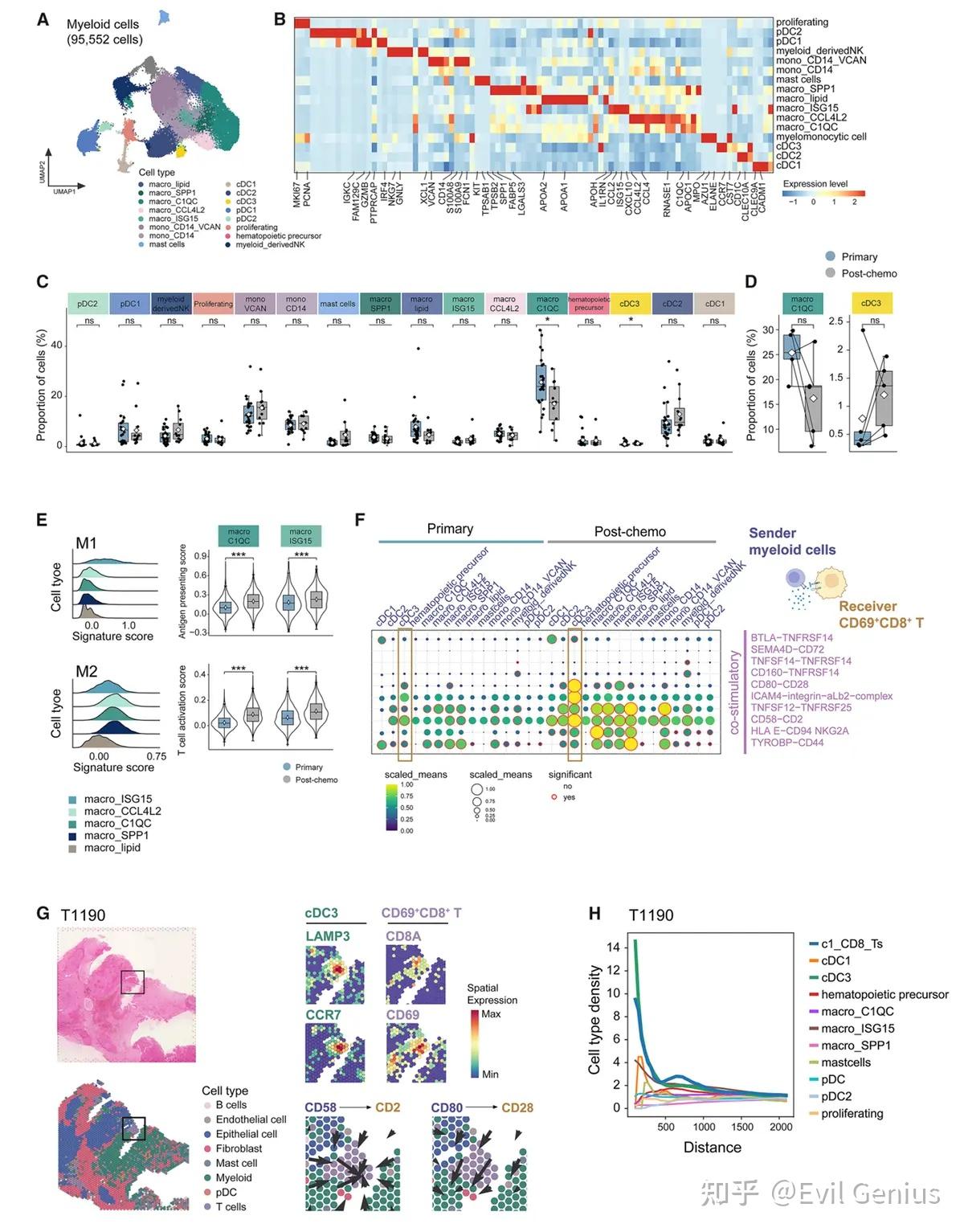
结果3、化疗后髓系细胞向免疫激活表型的重塑
化疗后髓系细胞亚群的比例变化
显著下降:Macro_C1QC(C1QC+巨噬细胞)在化疗后比例显著减少(5对配对样本中有4例下降)。
显著上升:cDC3(经典树突状细胞3)在化疗后比例显著增加(5对配对样本中有4例上升)。
巨噬细胞的表型与功能转变
M1/M2分型:
- Macro_C1QC、Macro_SPP1、Macro_CCL4L2偏向M2样表型(促肿瘤)。
- Macro_ISG15偏向M1样表型(抗肿瘤)。
化疗后功能变化:
- Macro_C1QC和Macro_ISG15在化疗后均上调了抗原呈递和T细胞活化相关基因。
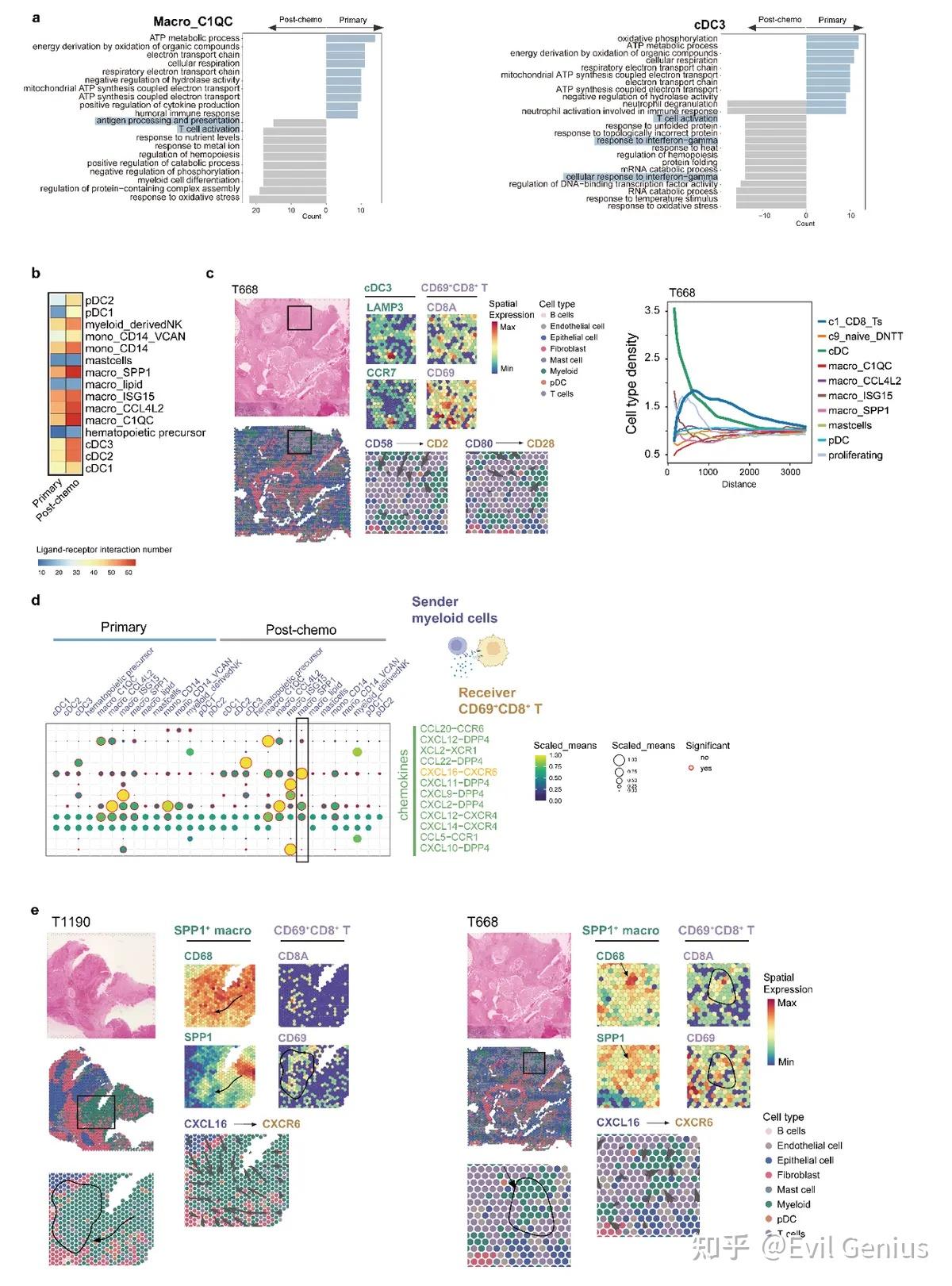
- 基因本体论分析显示,化疗后Macro_C1QC富集了T细胞活化和抗原呈递通路,提示其向免疫刺激环境转变。
- cDC3的变化:化疗后cDC3上调了T细胞活化和干扰素-γ应答通路相关基因,与化疗相关的有利免疫反应一致。
髓系细胞与CD69+ CD8+ T细胞的相互作用
相互作用增强:化疗后,多个髓系细胞亚群与CD69+ CD8+ T细胞之间的相互作用增强。
共刺激通路:髓系细胞(作为抗原呈递细胞)通过CD80-CD28和CD58-CD2等共刺激通路激活T细胞,这可能促进了CD69+ CD8+ T细胞的扩增。
空间转录组学验证
空间共定位:
- cDC3细胞(表达LAMP3、CCR7、CD58、CD80)与CD69+ CD8+ T细胞(表达CD2、CD28)在空间上共定位。
- 基于CD58-CD2和CD80-CD28配体-受体对的空间细胞间相互作用分析与空间邻近性一致。
- 量化分析证实CD69+ CD8+ T细胞与cDC3之间存在显著共定位。
- SPP1+巨噬细胞与CD69+ CD8+ T细胞之间通过CXCL16-CXCR6的通信也在化疗后增强,并证实其空间共定位。
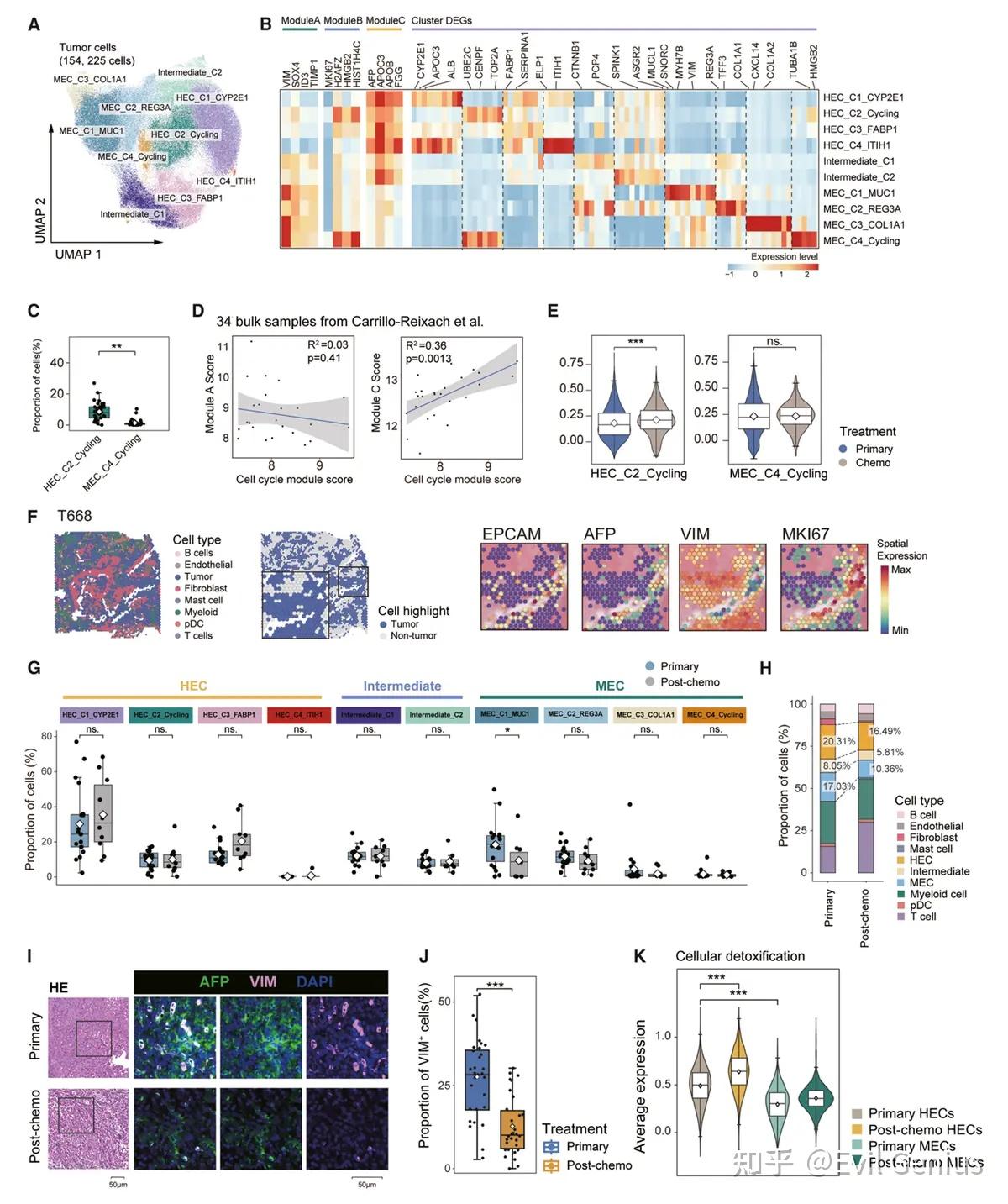
结果4、识别两种主要的肿瘤细胞亚型
肿瘤细胞亚型鉴定
数据基础:对154,255个上皮细胞进行亚聚类分析,得到12个亚群。
正常细胞排除:通过计算CNV评分和Wnt信号活性,排除2个正常上皮细胞亚群(低CNV、低Wnt信号)。
转录模块:通过非负矩阵分解和差异表达基因分析,鉴定出三个转录模块:
- 模块A(间质模块):特征基因VIM、ID3、SOX4。
- 模块B(细胞周期模块):特征基因TOP2A、MKI67。
- 模块C(肝细胞模块):特征基因AFP、GPC3、APOC3、APOB、FGG。
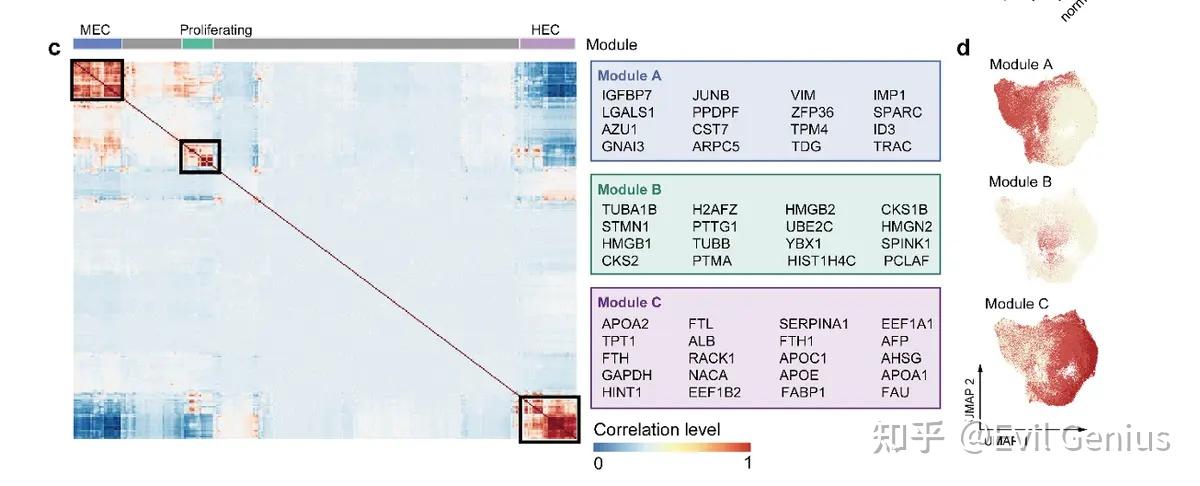
肿瘤细胞两大主要亚型
间质样细胞(MECs):高表达间质模块基因(VIM)。包括MUC1+亚群和COL1A1+亚群。
肝细胞样细胞(HECs):高表达肝细胞模块基因。其中部分亚群高表达肝细胞功能基因(CYP2E1、APOC3、ALB),代表更分化的状态。
中间状态:存在共表达肝细胞和间质特征的中间型细胞。
病理亚型相关性
胚胎型/混合型肿瘤:富集MECs(如MEC_C1_MUC1)。
纯胎儿型肿瘤:富集HECs。
增殖活性:循环HECs的比例在胚胎型肿瘤中最高,混合型居中,胎儿型最低。
增殖特征比较
增殖比例:循环HECs(18.0%)的增殖比例显著高于循环MECs(6.5%)。
数据验证:
- 在已发表的单细胞数据和bulk数据中均证实细胞周期模块与肝细胞模块正相关,与间质模块不相关。
- 空间转录组数据显示高增殖区域高表达AFP、低表达VIM。
化疗后变化:化疗后,循环HECs的增殖活性显著增加,而循环MECs无显著变化。
分化状态:RNA速率拟时序分析显示,循环HECs处于最低拟时序评分,代表 progenitor 状态。
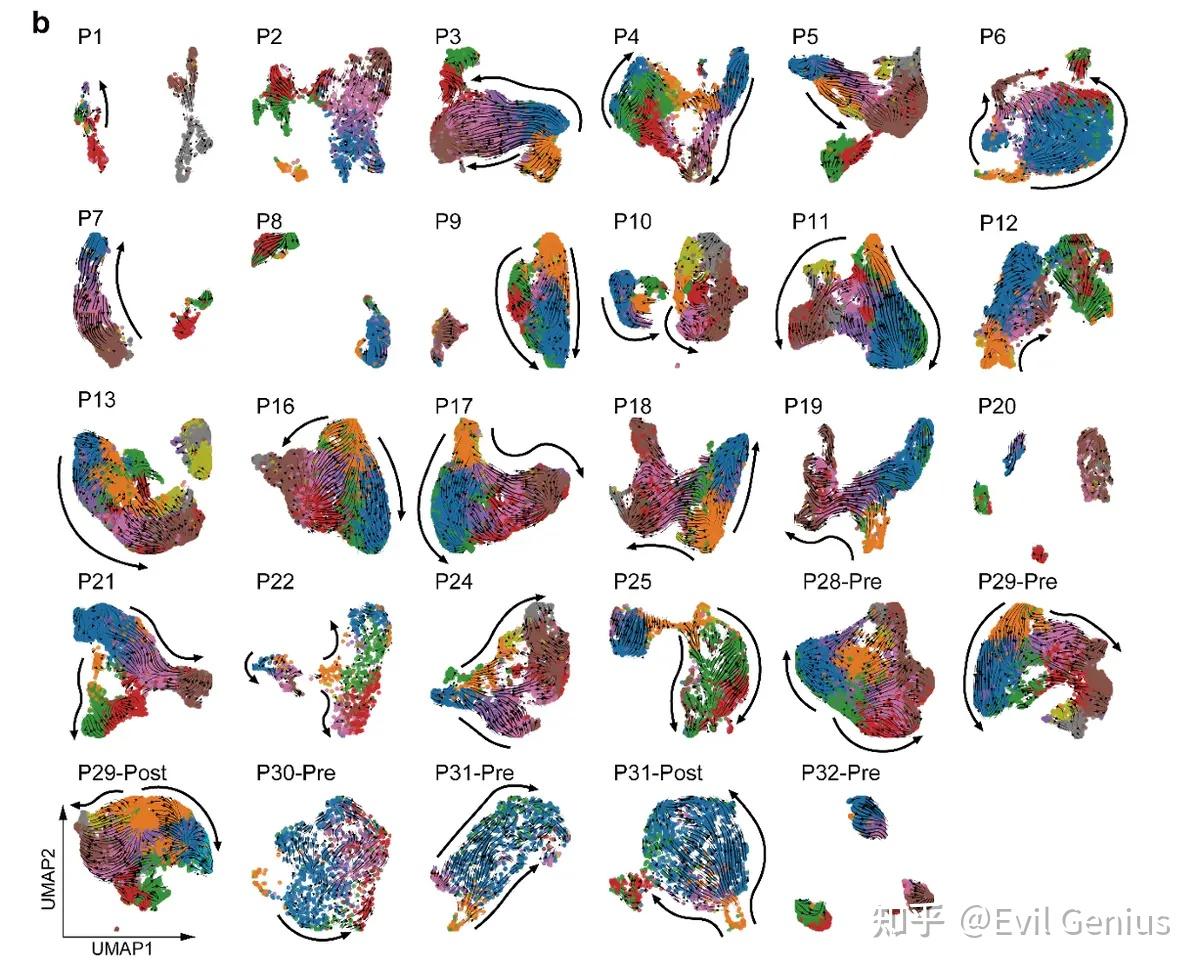
基因组影响
CNV分析显示,大多数病例的肿瘤细胞具有相似的CNV水平和模式。
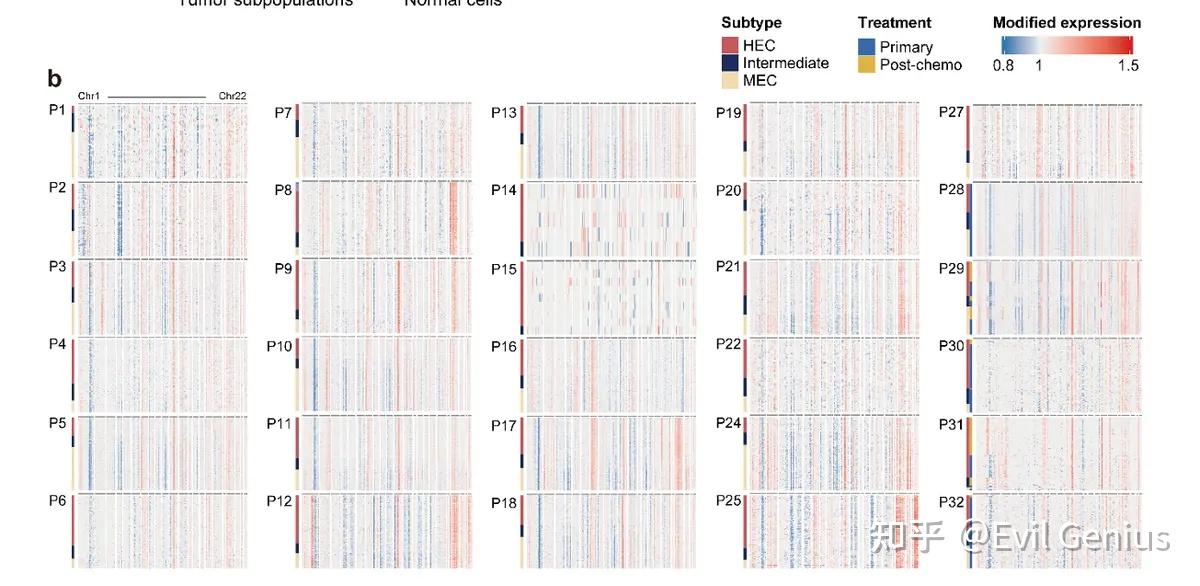
肿瘤细胞亚群比例与CNV评分之间关联性弱,提示表型多样性可能不完全由基因组CNV决定。
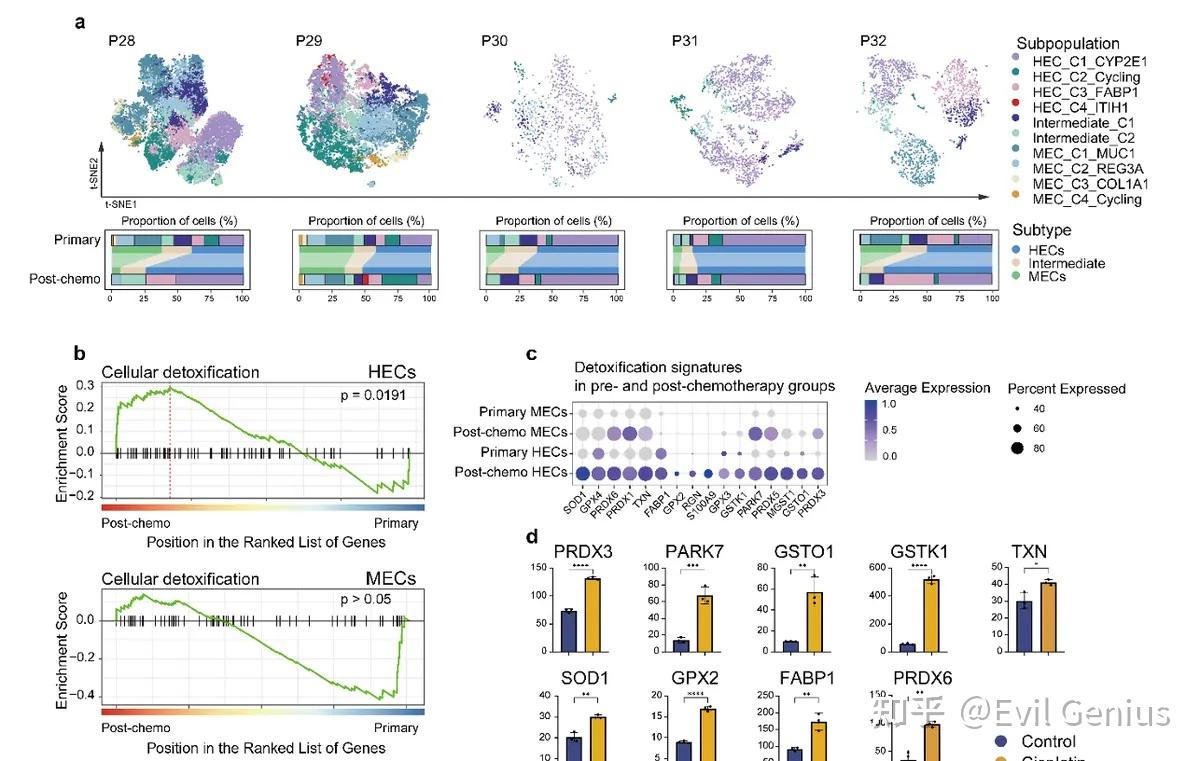
化疗后肿瘤细胞亚型的比例变化
预期 vs 实际:尽管HECs(肝细胞样细胞)增殖比例更高(理论上更易被化疗杀伤),但化疗后其比例并未显著减少;而MECs(间质样细胞)的比例则显著下降。
通路富集分析:对5例配对患者的纵向肿瘤细胞分析显示,化疗后的HECs显著上调了细胞解毒通路相关基因,而MECs中未观察到这一现象。
HECs在化疗后表现出更强的细胞解毒特征上调,这可能是其对化疗更具耐药性的原因之一。
MECs对化疗更敏感,化疗后比例显著下降。
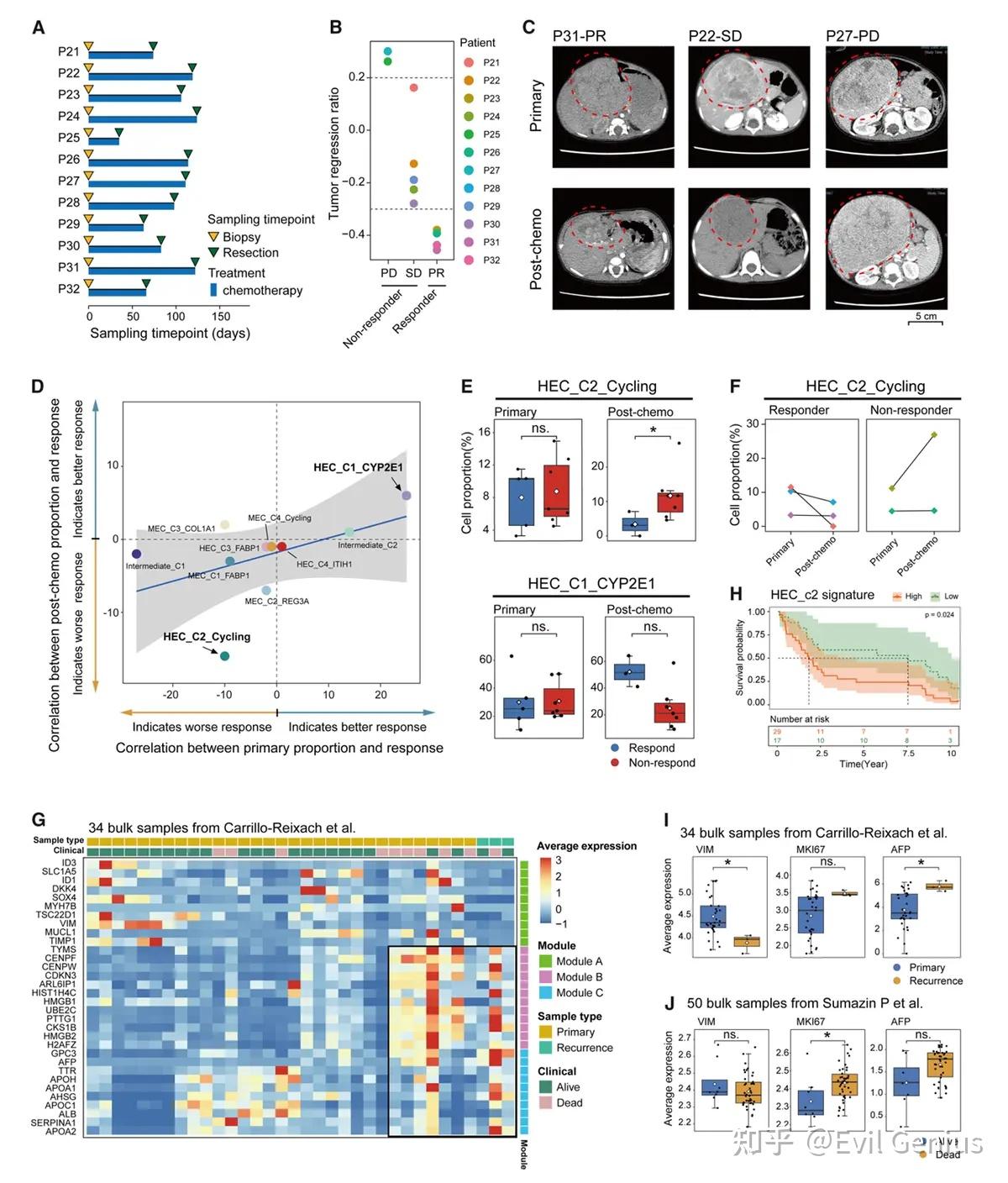
结果5、高度增殖的HECs可能在化疗后介导肿瘤复发
肿瘤细胞亚群与化疗反应的关系
预测不良反应的亚群:增殖性HECs(HEC_C2)是最能预测化疗不良反应的肿瘤细胞亚群。无应答者在化疗后该亚群比例显著更高。
纵向变化:5例配对数据显示,3例应答者中增殖性HECs普遍减少;2例无应答者中该亚群比例增加(其中一例从11.2%升至26.9%)。
与良好反应相关的亚群:分化型HECs(HEC_C1)似乎与化疗良好反应相关。
肿瘤微环境细胞与化疗反应的关联(初步观察)
与不良反应相关(比例增加):Tex、Tregs、C1QC+巨噬细胞/单核细胞、MMP11+ CAF。
与良好反应相关(比例增加):CD69+ CD8+ T细胞、pDC、cDC。
说明:这些差异未达统计学显著性,可能受样本量限制。
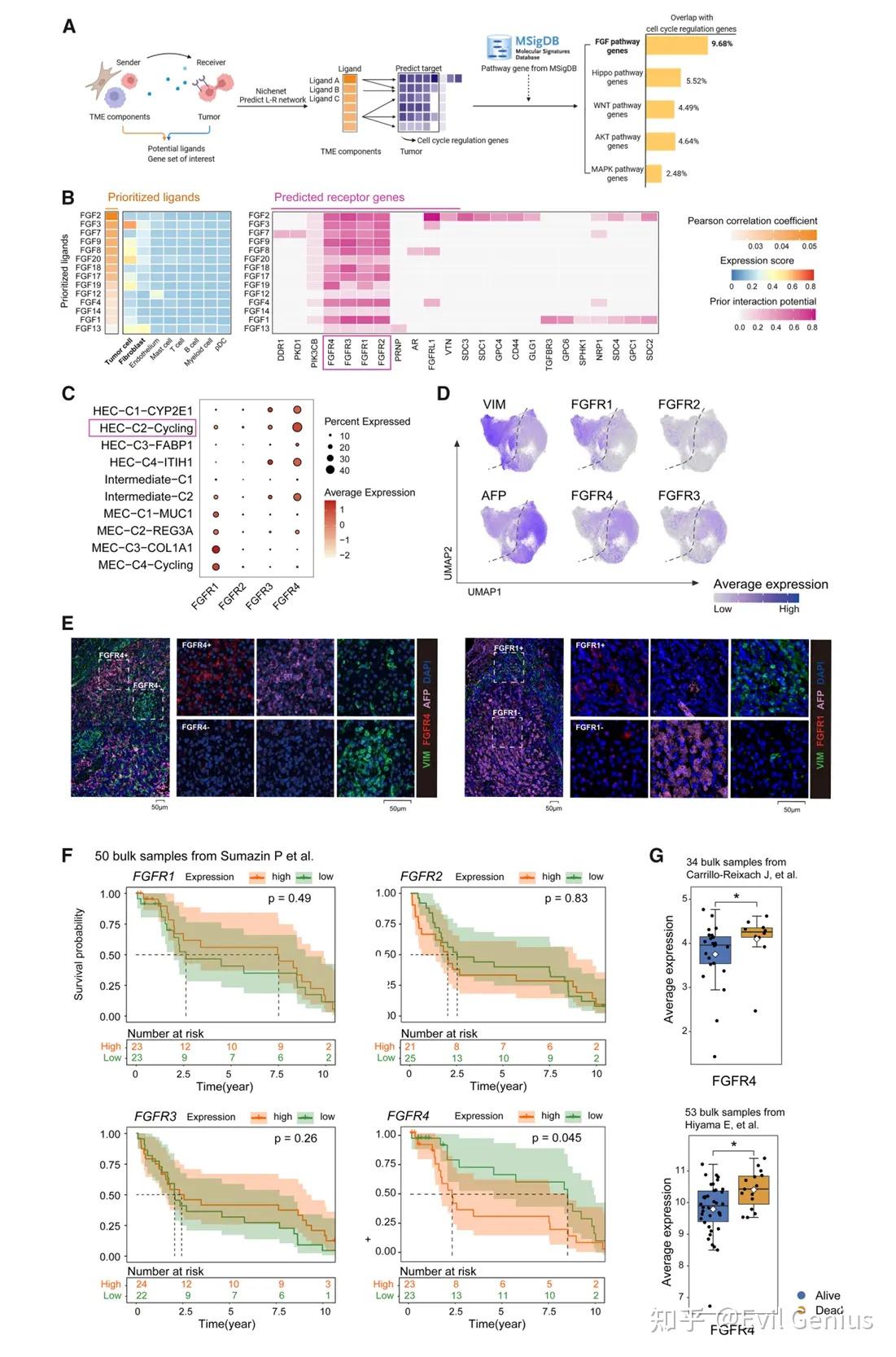
结果6、与肿瘤细胞增殖相关的细胞间相互作用网络
运用NicheNet算法构建肿瘤细胞与肿瘤微环境其他组分之间的配体-受体网络,系统分析影响肿瘤细胞增殖的细胞间通讯。
核心发现:FGF-FGFR信号通路与肿瘤细胞增殖存在 robust 关联。
自分泌:肿瘤细胞自身高表达多种FGFs。
旁分泌:成纤维细胞高表达多种FGFs,提示成纤维细胞可通过旁分泌方式向肿瘤细胞传递FGFR信号。
FGFRs在肿瘤细胞亚型中的差异表达
表达模式:
HECs(肝细胞样细胞):主要表达FGFR4。
MECs(间质样细胞):主要表达FGFR1。
实验验证:通过多重免疫组化染色证实了FGFR4在AFP+ VIM- HECs中表达,FGFR1在AFP- VIM+ MECs中表达。
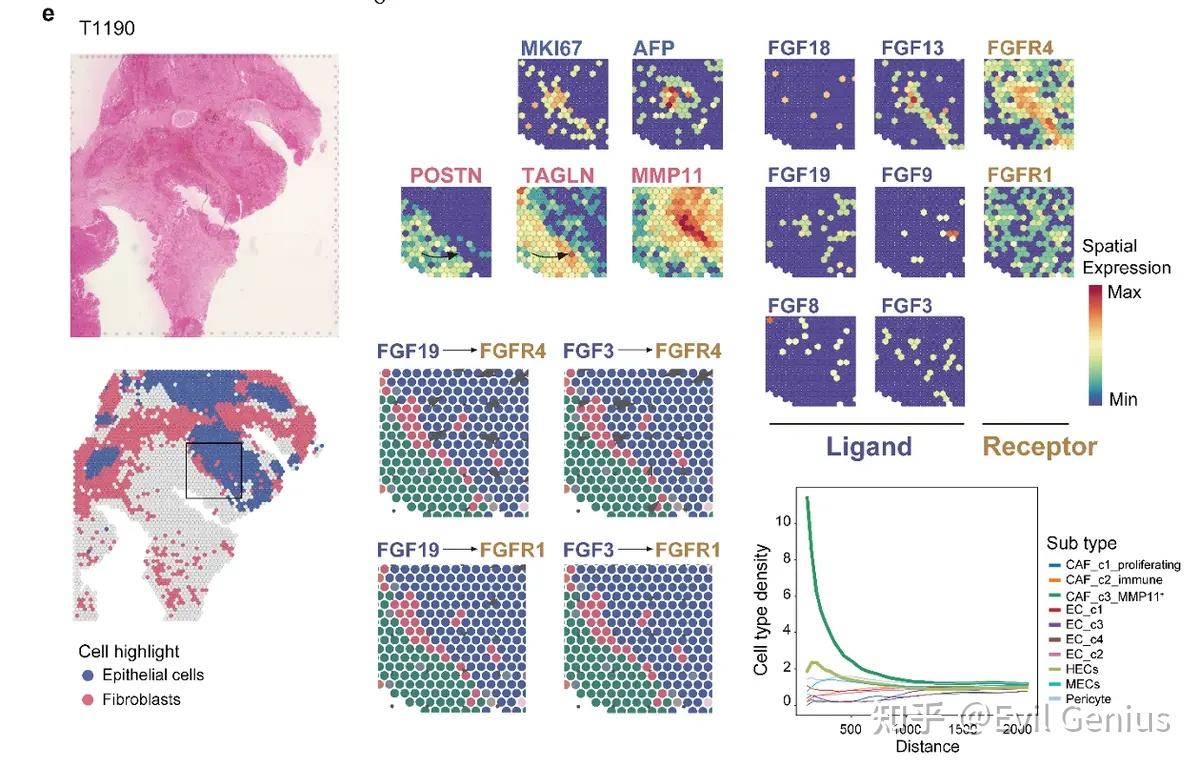
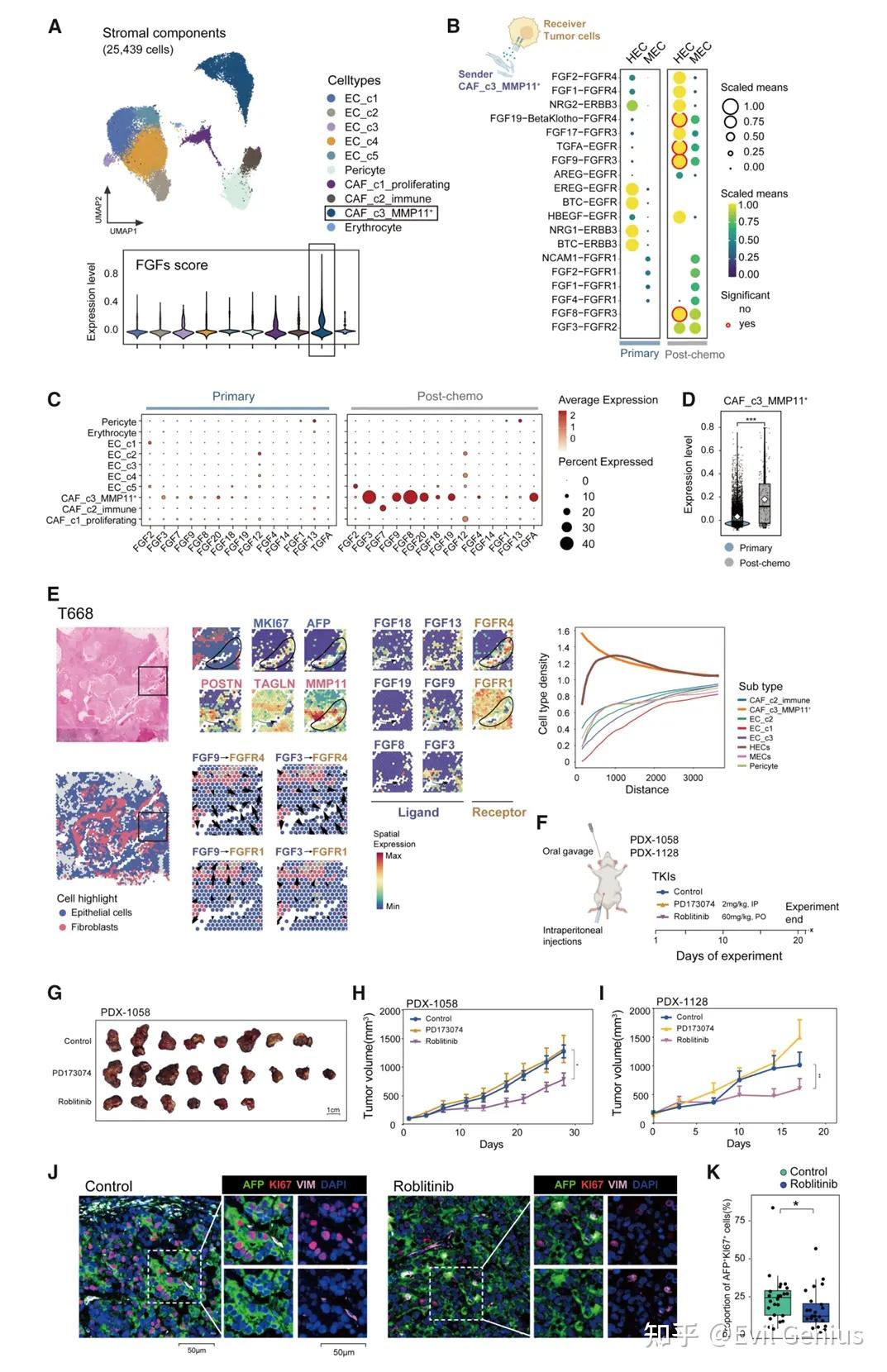
结果7、化疗后FGF信号由MES肿瘤细胞和MMP11+CAF增强
化疗后,间质样肿瘤细胞(MECs)和MMP11+癌症相关成纤维细胞(CAFs)共同增强了FGF-FGFR信号通路的激活。具体而言,MECs在化疗后上调了多种FGF配体的表达;而MMP11+ CAFs则高表达FGF3和FGF8,并与表达FGFR4的增殖性肝细胞样肿瘤细胞(HECs)在空间上共定位,通过FGF3-FGFR4等信号对在化疗后形成更活跃的旁分泌通讯,提示这种由MECs和特定CAFs亚群介导的FGF信号增强可能促进了HECs的增殖并参与化疗耐药。基于此,使用FGFR4抑制剂罗泊替尼在患者来源的异种移植模型(以AFP+ HECs为主)中显著抑制了肿瘤生长,减少了增殖性肿瘤细胞,且在低剂量化疗联用时表现出协同增效作用。
最后,来看看方法

空间通讯和轨迹分析

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

