HD文章分享--肝细胞癌早期恶变的分子机制研究
原创HD文章分享--肝细胞癌早期恶变的分子机制研究
原创
追风少年i
发布于 2026-03-31 10:07:49
发布于 2026-03-31 10:07:49
作者,Evil Genius
生活不易,有空的时候,敬一杯给自己。
无论之前做了什么决定,多么后悔,但是一个男人,只能勇敢的往前走,30多岁,尤其结了婚的,都要负重前行了。
越长大,越孤独,越没人理解,越没有朋友,反倒是各种恶言恶语、不利环境需要自己承受,肉眼可见短期内都越来越难,而且也越来越深刻体会,苦命人往往为难苦命人,都是社会底层,反倒是相互伤害。
2026真的是,你好老己。
今天我们分享文献,经过这几年,我是发现了,科研这条路,需要点天赋,有的人学完半年多文章就见刊了,速度真的快。看文献的作用就类似感冒多喝热水,喝的多了,思路有了,再用代码实现。
HD文章已经很多了,我们就不再排序了。

知识积累
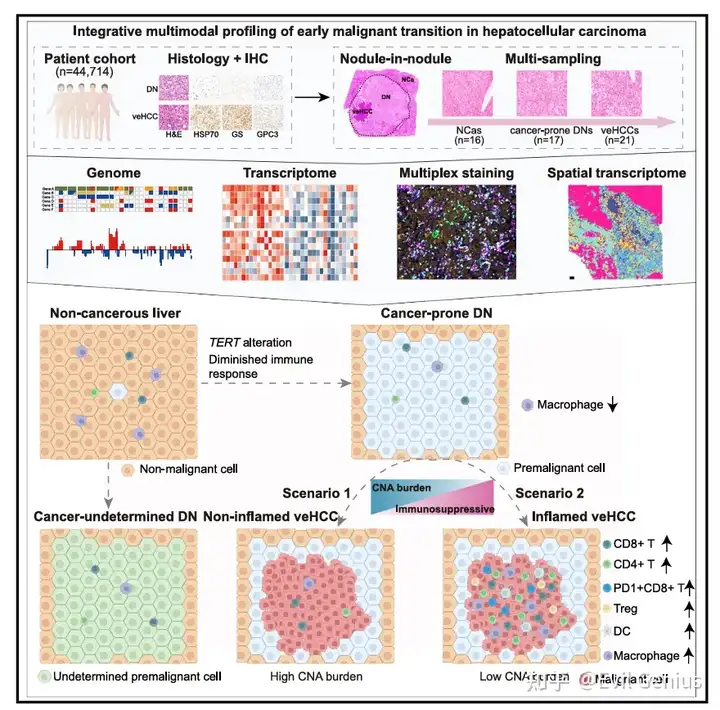
肝细胞癌通常起源于不典型增生结节,这是一种癌前病变,估计有30%的风险进展为肝细胞癌。以往的研究使用无演化关系的不典型增生结节和肝细胞癌分析了肝癌的起始过程。这里利用“结节内结节”病变这一独特机会,深入研究不典型增生结节内极早期肝细胞癌(veHCCs)的发生发展过程。
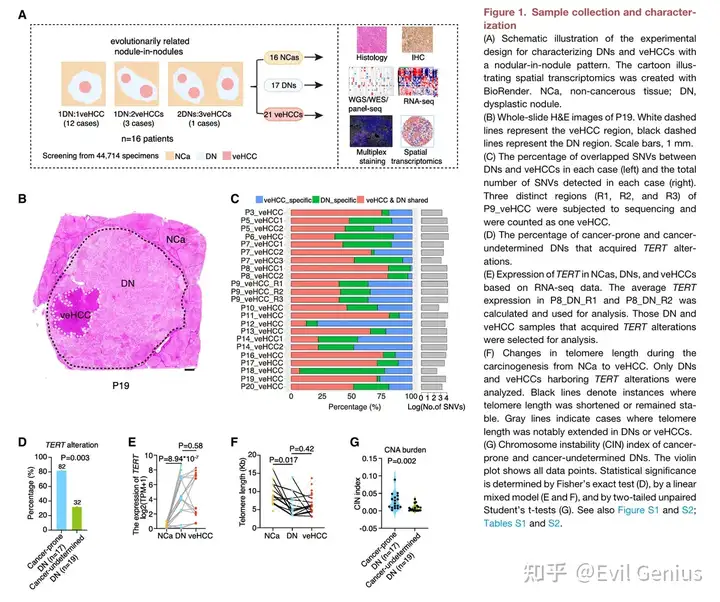
结果1、样本来源
样本进行了全基因组测序(WGS,约35×覆盖度)和RNA测序。17个不典型增生结节(称为"癌 prone 不典型增生结节")与其演化相关的极早期肝细胞癌(共21个极早期肝细胞癌)共享了7%–85%的单核苷酸变异(SNVs)。值得注意的是,配对的不典型增生结节和极早期肝细胞癌表现出相似的突变特征模式。此外,来自患者3(P3)的后续磁共振成像(MRI)数据验证了该病例中从不典型增生结节到极早期肝细胞癌的演化过程。这些数据共同证明了它们之间的演化关系。
为确认能否从FFPE样本中捕获单核苷酸变异,我们比较了两个肝细胞癌样本在新鲜冷冻组织和FFPE组织中的单核苷酸变异谱。与先前报道的方法一致,在新鲜冷冻样本中检测到的94.4%的单核苷酸变异在FFPE组织中得到确认,表明FFPE组织在很大程度上保留了原始的单核苷酸变异。
为识别癌前病变恶性转化的关键分子事件,研究者从19名乙肝病毒感染者处获取了19个无原位癌病变、癌变潜能未定的不典型增生结节(简称“癌未定DN”)及其配对非癌组织作为对照,与癌 prone DN(即与极早期肝细胞癌具演化关系的DN)进行比较分析。基于8个已发表的肝细胞癌队列所编目的37个肝癌功能基因列表进行分析后发现,TERT基因变异(包括HBV整合、启动子突变及拷贝数增加)在癌 prone DN中的检出率高达82%,显著高于癌未定DN的32%(p = 0.003),提示TERT变异虽在癌 prone DN中高度普遍,但并非恶性转化的直接驱动因素。尽管TERT变异在癌 prone DN及匹配的极早期肝细胞癌中均上调了TERT表达,但携带该变异的癌 prone DN中仍有79%表现为端粒显著缩短,且这一趋势在TERT表达升高的亚组中同样持续存在(73%,8/11),同时在65%的极早期肝细胞癌中端粒长度也未恢复甚至进一步缩短,表明即使在TERT变异存在的情况下,端粒损耗仍持续贯穿恶性转化过程。此外,与癌未定DN相比,癌 prone DN中拷贝数变异显著富集(p = 0.002),其中以Chr7p(EGFR)、Chr7q(MET)和Chr8q(MYC)的增益最为突出,分别占24%、24%和12%,提示这些拷贝数变异可能在推动癌前病变向恶性转化中发挥关键作用。
结果2、拷贝数变异与恶性转化密切相关
在从不典型增生结节(DN)向极早期肝细胞癌(veHCC)的恶性转化过程中:
SNV负荷无显著变化:与配对的癌前DN相比,veHCC中的总SNV及蛋白质改变性SNV数量均无显著增加,表明DN-to-veHCC的转化与SNV负荷无关。虽然少数veHCC获得了新的肝癌功能基因突变(如ARID1A),但71%的veHCC未见此类获得性SNV。此外,veHCC中TP53和CTNNB1的突变频率显著低于晚期HCC。
CNA负荷显著增加:与配对DN相比,veHCC的CNA负荷(>1 Mb)显著更高,且89%的臂水平CNA(如Chr1q增益、Chr10q缺失)在veHCC中频率增加。veHCC特有10个携带肝癌功能基因的CNA(如TSC1、RB1缺失和KRAS增益),其中部分CNA在晚期HCC中仍以相当频率存在。
存在渐进性CNA事件:在19%的veHCC中检测到Chr1p(15–28 Mb)大片段特有缺失,而配对DN仅表现为相邻区域的较短缺失,提示该区域存在恶性转化过程中的渐进性缺失。该区域包含ARID1A和NR0B2两个肿瘤抑制基因,且在veHCC中表达下调。
CNA驱动恶性转化的多重证据:veHCC中癌基因增益和肿瘤抑制基因缺失均多于配对DN,同时伴有染色体不稳定性相关基因表达上调、DNA修复及染色体断裂特征增强。TP53变异在高染色体不稳定性veHCC中显著富集。
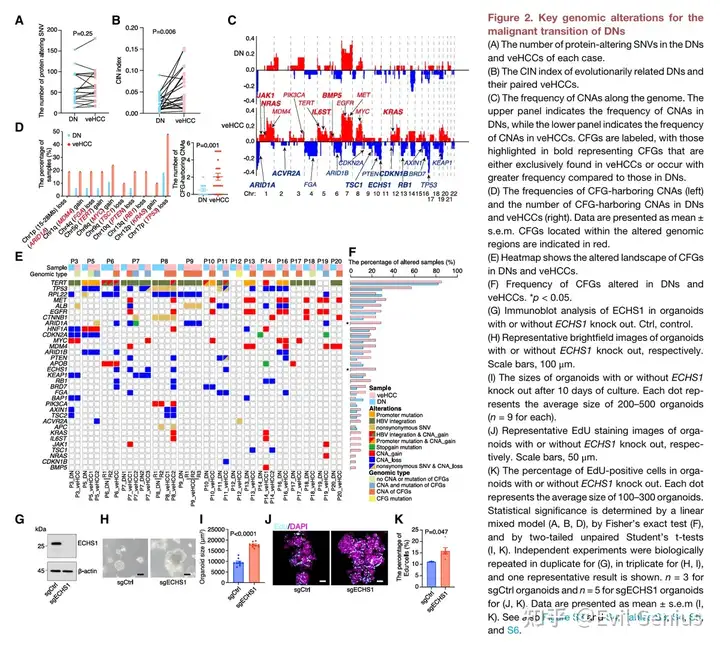
从不典型增生结节到恶性转化的关键遗传改变
整合分析揭示CNA的主导地位:
在分析的37个肝癌功能基因(CFG)中,33个在癌 prone DN与配对veHCC中存在改变。
83%的veHCC在CFG中获得了额外的CNA(其中61%仅有CNA获得而无额外突变,22%同时获得CNA与突变),而仅有一个veHCC获得了额外的CFG突变但无CNA。
在veHCC中,由CNA诱导的CFG改变数量显著高于SNV诱导的CFG改变数量,进一步证明CNA是恶性转化的主要驱动力。
veHCC特有的CFG改变:
11个CFG的改变仅在veHCC中检测到,其中ARID1A改变(拷贝数缺失或功能丧失突变)见于6个veHCC,ECHS1拷贝数缺失见于5个veHCC,提示这些基因可能在恶性转化后期发挥作用。
类器官模型的功能验证:
通过人诱导肝细胞(hiHep)类器官模型,验证了c-MYC和CTNNB1激活可显著促进类器官生长,与临床观察一致。
对7个候选基因的功能评估显示,ECHS1缺失和FGA下调均能显著促进类器官增殖(增大尺寸、提高EdU阳性细胞比例),为这两个基因在肝癌早期恶性转化中的驱动作用提供了直接实验证据。
结果3、癌前不典型增生结节中的免疫荒漠表型
癌 prone DN 与癌未定 DN 的差异有限:两者之间仅鉴定出52个差异表达基因,其中癌 prone DN 上调的基因富集于代谢过程,而癌未定 DN 上调的基因中多为功能未明的 snoRNA,提示两者在转录组层面的差异相对较小。
从 DN 到 veHCC 的转录组动态变化分为三个模块:
模块1(增殖相关):表达逐渐升高,但 DN 中细胞周期基因诱导的同时伴随 CDKN2A 上调,因此增殖细胞(Ki67阳性)仅在 veHCC 中显著增加。
模块2(代谢相关):表达逐渐降低,涉及肝脏特异性代谢功能(如脂肪酸、维生素代谢)的丧失,以及糖酵解的增强,提示代谢重编程。
模块3(微环境相关):呈现先降后升的模式,富集于上皮-间质转化、血管生成和免疫相关通路,反映恶性转化过程中微环境的动态变化。
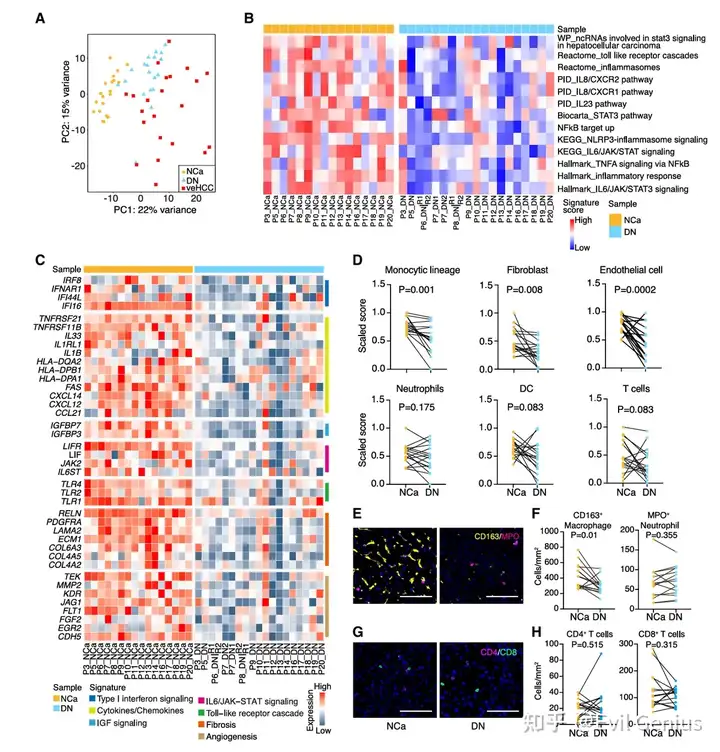
癌 prone DN 表现为免疫失活的“荒漠”状态:
炎症信号下调:促炎性细胞因子(如IL1B、IL33)、I型干扰素、Toll样受体以及炎症相关纤维化和血管生成基因的表达均显著降低,且这种低炎症特征在大部分癌未定 DN 中也存在。
免疫细胞浸润减少:通过反卷积分析和多重染色证实,癌 prone DN 中成纤维细胞、内皮细胞、巨噬细胞(CD163+)及T细胞(CD4+、CD8+)的丰度均显著低于非癌组织和晚期 HCC。
悖论:尽管晚期 HCC 常与炎症相关,但其癌前病变阶段(癌 prone DN)却处于免疫抑制/荒漠状态,提示恶性转化可能是在免疫监视缺失的“冷”环境中启动的。
结果4、炎症型极早期肝细胞癌的免疫逃逸表型
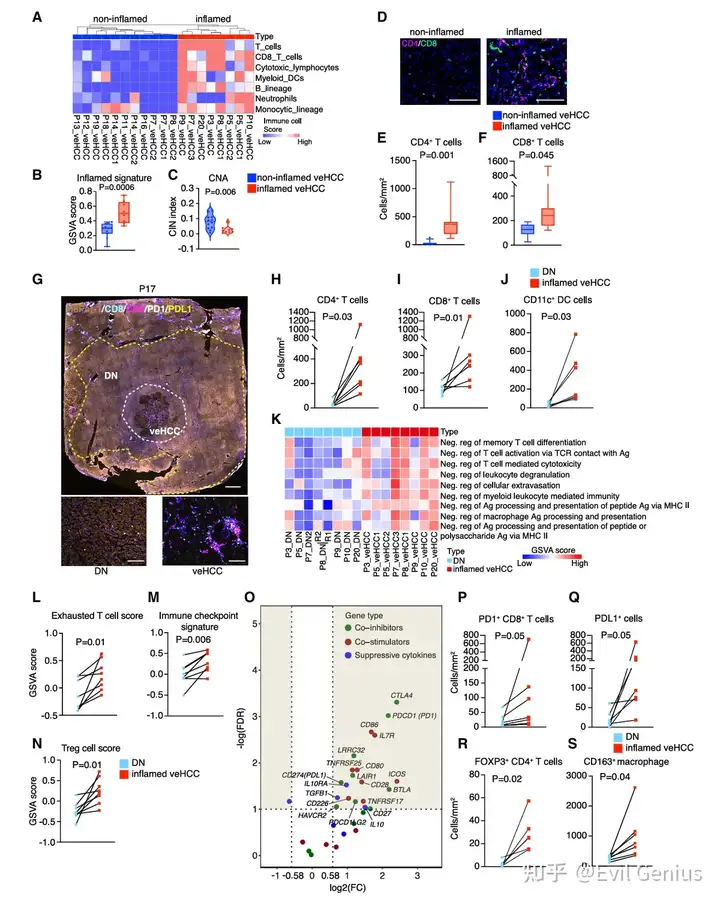
为明确极早期肝细胞癌(veHCC)的免疫特征,研究者评估了免疫细胞丰度及20个核心基因构成的炎症特征激活评分。结果显示,43%的veHCC同时表现出T细胞和树突状细胞高浸润及炎症特征富集,被定义为“炎症型veHCC”。
两种主要亚型:整合转录组与基因组特征揭示了veHCC的两个亚型——低拷贝数变异负荷的炎症型与高拷贝数变异负荷的非炎症型。炎症型veHCC的染色体不稳定性指数更低,拷贝数变异负荷显著减少,而单核苷酸变异负荷及新抗原水平在两类间无差异。
免疫激活特征:与非炎症型相比,炎症型veHCC高表达趋化因子(如CXCL12、CCL2、CCL5)、HLA II类分子及免疫细胞标志物(CD3D、CD4、CD8A),且通过多重染色证实CD4+和CD8+ T细胞高度浸润。与其配对的癌前不典型增生结节相比,炎症型veHCC的适应性免疫细胞标志物及T细胞、树突状细胞丰度均显著提升。
伴随早期免疫逃逸:尽管免疫被激活,炎症型veHCC同时表现出免疫逃逸特征——与配对不典型增生结节相比,T细胞负调控、抗原加工提呈相关通路已上调。其免疫抑制相关特征评分显著升高,包括耗竭性T细胞、免疫检查点(CTLA4、PDL1、PD1)、调节性T细胞(FOXP3+)、M2型巨噬细胞及肿瘤相关巨噬细胞特征。免疫组化进一步证实PD1+CD8+ T细胞、PDL1+细胞、FOXP3+CD4+ T细胞及CD163+巨噬细胞浸润增加。
信号通路与代谢特征:炎症型veHCC富集IL6、TNF-α、上皮-间质转化、KRAS等致癌驱动通路,同时胆汁酸通路相关基因下调(已知胆汁酸可抑制T细胞应答)。
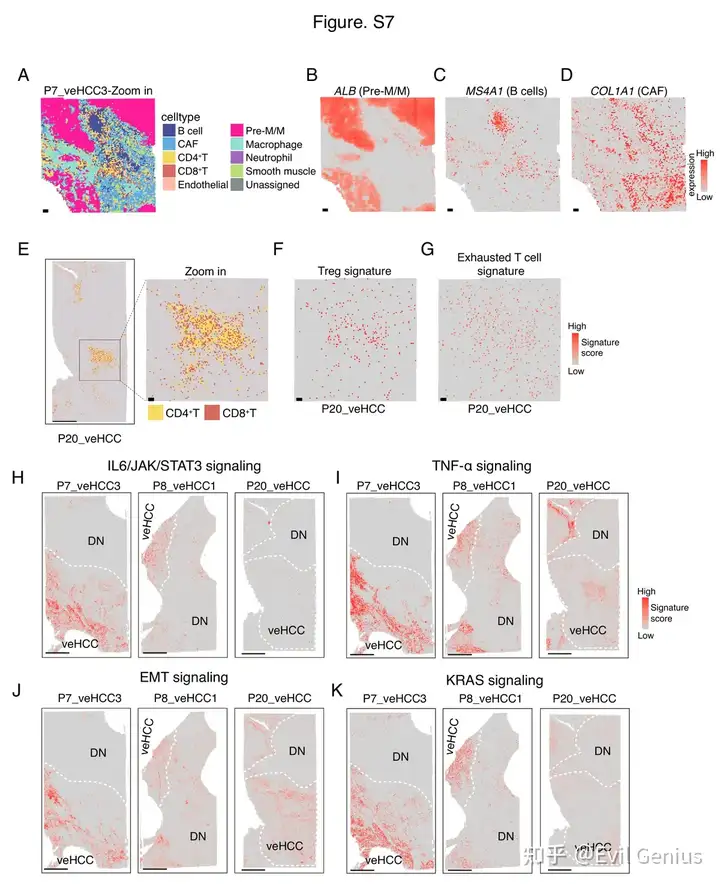
结果5、炎症型极早期肝细胞癌免疫表型的空间定位
visium HD
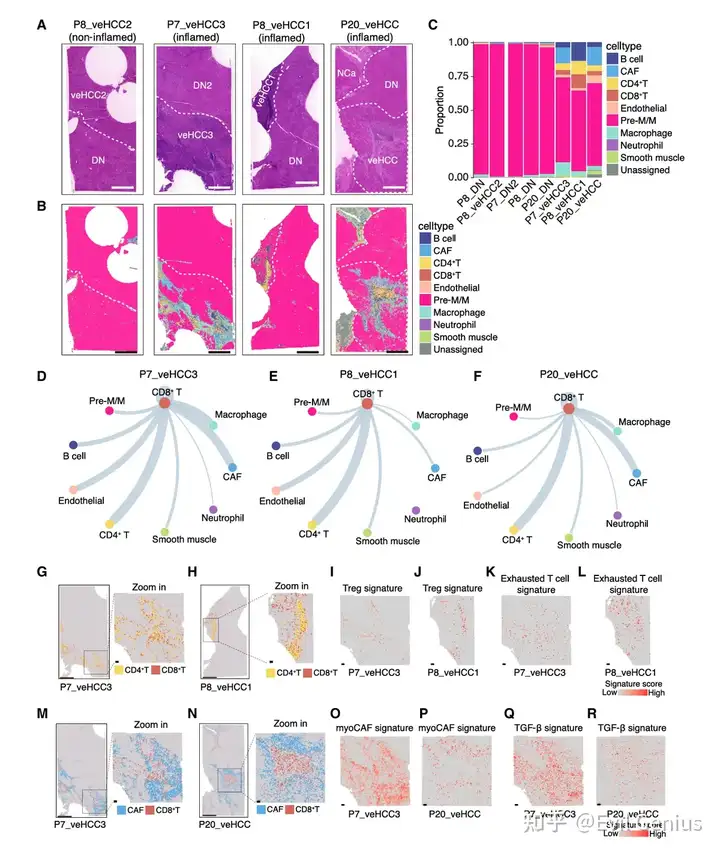
细胞类型与浸润特征:
炎症型极早期肝细胞癌相比配对不典型增生结节,CD4+ T细胞、CD8+ T细胞、巨噬细胞和B细胞的丰度增加,其中2例中癌症相关成纤维细胞显著增多。
相比之下,非炎症型极早期肝细胞癌及其配对不典型增生结节始终呈现低免疫细胞和基质细胞浸润。
细胞间相互作用:
CD8+ T细胞与多种细胞类型存在广泛相互作用,其中与CD4+ T细胞的配体-受体相互作用数量最多。
空间上,CD4+与CD8+ T细胞紧密相邻,形成 distinct 细胞簇,这些区域中调节性T细胞和耗竭性T细胞特征评分显著升高。
免疫抑制微环境的建立:
癌症相关成纤维细胞是与CD8+ T细胞相互作用的顶级细胞类型之一,二者在空间上邻近。在癌症相关成纤维细胞和CD8+ T细胞富集的区域,肌成纤维细胞癌症相关成纤维细胞和TGF-β特征显著激活,支持TGF-β介导的免疫抑制作用。
CD8+ T细胞与巨噬细胞之间存在相互作用,与炎症型极早期肝细胞癌中肿瘤相关巨噬细胞浸润增加的多重染色结果一致。
信号通路激活:
炎症型极早期肝细胞癌中IL6、TNF-α、上皮-间质转化和KRAS等致癌通路被激活,与整体RNA-seq分析结果一致。
空间转录组学数据揭示了炎症型极早期肝细胞癌的免疫微环境特征——在激活炎症信号的同时,通过CD4+ T细胞与CD8+ T细胞的协同聚集、癌症相关成纤维细胞与TGF-β介导的抑制、以及肿瘤相关巨噬细胞的浸润,从空间上建立了多重免疫抑制网络,为理解极早期肝癌的免疫逃逸机制提供了空间维度的直接证据。
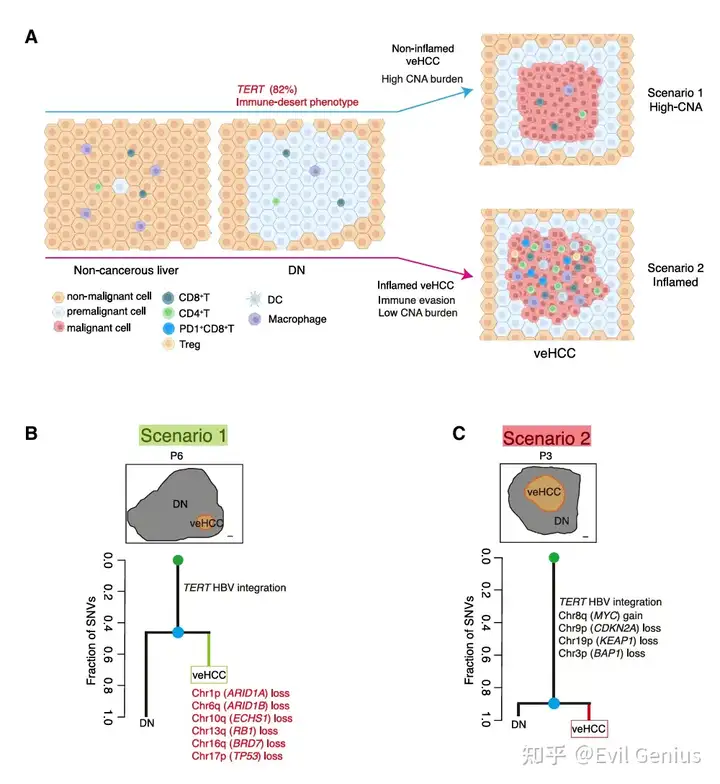
结果6、恶性转化演化场景的综合分析
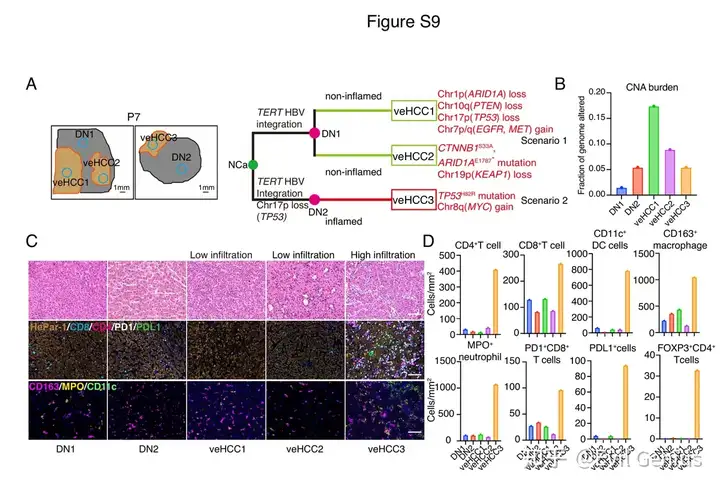
在肝细胞癌(HCC)发生的早期阶段,既存在基因组改变,也发生免疫微环境变化。TERT基因变异和免疫应答减弱是癌 prone 不典型增生结节(DN)发生的关键事件。基于整合的基因组和免疫谱分析,研究者提出了从不典型增生结节向极早期肝细胞癌(veHCC)恶性转化的两种潜在演化场景:
场景1:拷贝数变异主导的进展型
特征为在恶性转化过程中积累大量拷贝数变异(CNA),导致肝癌功能基因(CFG)发生广泛改变
对应非炎症型veHCC,免疫浸润水平低
代表性病例P6和P14显示:主干事件为TERT变异,分支事件中积累了大量携带肝癌功能基因的拷贝数变异(如TP53、RB1、ARID1A缺失,KRAS增益等)
场景2:伴随免疫逃逸的炎症进展型
对应炎症型veHCC,呈现免疫激活与免疫逃逸并存的特征
9例炎症型veHCC中,6例在恶性转化过程中获得了拷贝数变异诱导的肝癌功能基因改变,但拷贝数变异积累程度显著低于场景1
值得注意的是,3例炎症型veHCC(P3_veHCC、P5_veHCC1、P8_veHCC1)与其配对不典型增生结节呈现几乎相同的拷贝数变异谱,且未在37个肝癌功能基因中获得额外突变,提示免疫逃逸本身可能在缺乏关键基因突变的情况下驱动恶性转化
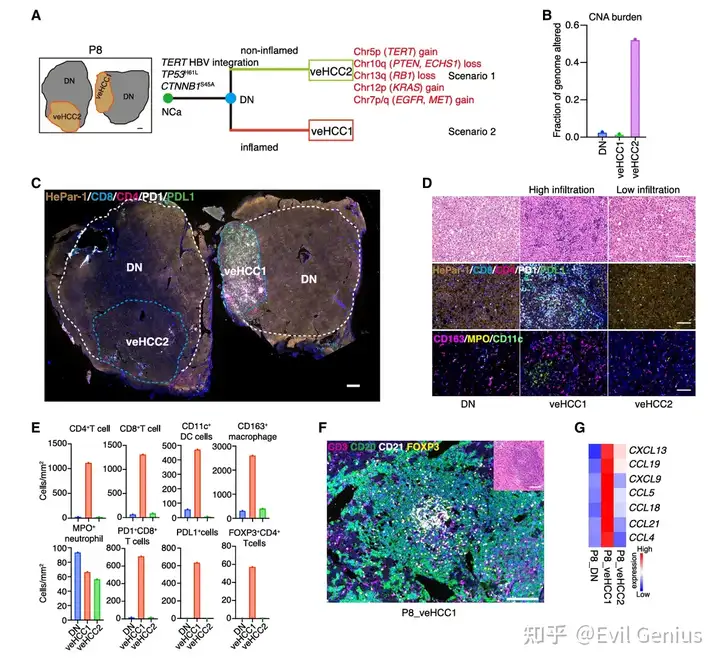
同患者多灶性病变的演化异质性
病例P8尤为典型:同一不典型增生结节内产生了两种演化路径的空间分离veHCC
P8_veHCC2:遵循场景1,积累了覆盖14条染色体的大量拷贝数变异,获得EGFR、MET、KRAS等癌基因增益,丢失PTEN、RB1等抑癌基因
P8_veHCC1:遵循场景2,拷贝数变异谱与配对不典型增生结节几乎相同,但呈现炎症表型,并形成三级淋巴结构,伴随PD1+CD8+ T细胞、FOXP3+CD4+ Treg细胞和PDL1+细胞浸润增加
总结:本研究提出了早期肝癌发生的两种演化路径——一种以拷贝数变异积累为主导驱动恶性转化,另一种则依赖于免疫逃逸机制的建立(即使缺乏关键基因突变的积累)。这两种场景可共存于同一患者的异质性病变中,揭示了肝癌早期演化的复杂性和多样性。
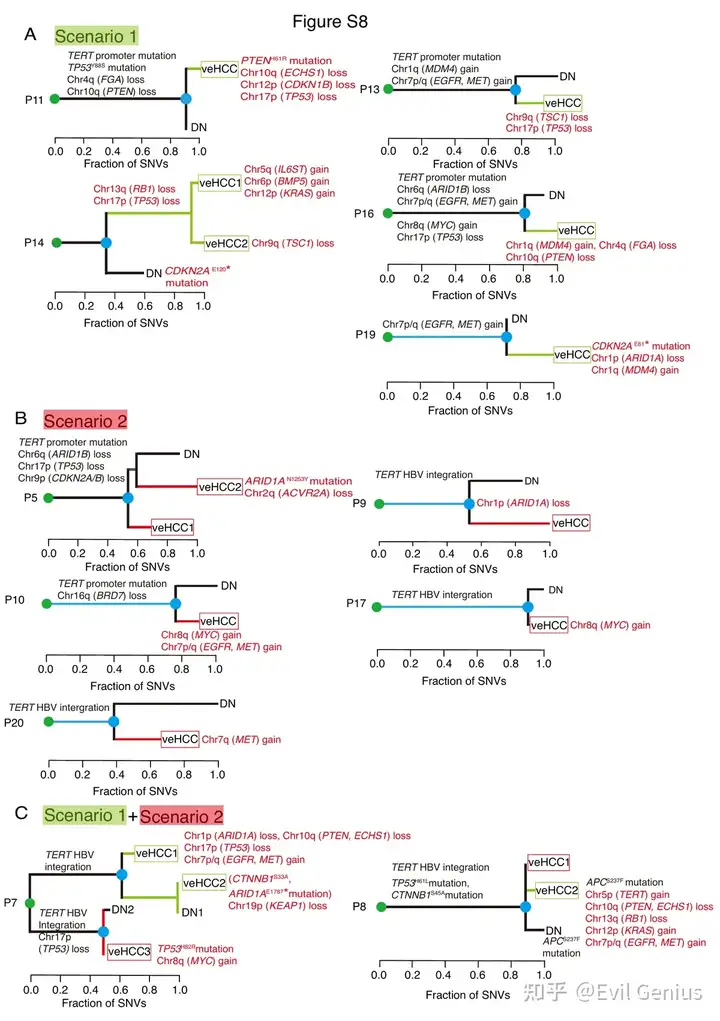
最后,来看看方法
visium HD

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

