Immunity | 单细胞+Xenium空间转录组揭示前列腺组织驻留记忆CD8+ T细胞的分化与异质性
Immunity | 单细胞+Xenium空间转录组揭示前列腺组织驻留记忆CD8+ T细胞的分化与异质性

生信大杂烩
发布于 2026-04-13 18:19:17
发布于 2026-04-13 18:19:17
论文标题:Distinct tissue niches contribute to prostate tissue-resident memory CD8+ T cell differentiation and heterogeneity 发表期刊:Immunity (2026) 通讯作者:Miguel Reina-Campos(La Jolla免疫学研究所)& Ananda W. Goldrath(UCSD / Allen免疫学研究所) DOI:10.1016/j.immuni.2026.03.003
一、研究背景
组织驻留记忆CD8+ T细胞(Tissue-resident memory T cells, Trm)是定位于非淋巴组织中的一群长寿命记忆T细胞,它们无需再循环即可在病原体入侵的第一时间提供快速的局部免疫保护。过去十年中,Trm细胞生物学已在肠道、肺、肾脏、肝脏、皮肤、唾液腺(SG)和白色脂肪组织(WAT)等屏障组织中得到了深入研究。这些研究揭示了Trm细胞的核心特征:上调组织驻留转录调控因子(如Runx3)、表达组织滞留分子(CD69和CD103),以及下调淋巴归巢因子(S1PR1、CD62L)以阻止组织外流。
然而,前列腺——作为男性生殖系统中重要的外分泌腺和屏障组织,同时也是恶性肿瘤的高发部位——其CD8+ T细胞群体的特征几乎完全未知。前列腺组织暴露于独特的细胞和代谢因素组合中,包括高浓度的TGFβ和雄激素,这些因素如何影响Trm细胞的形成和维持?前列腺内部是否存在空间离散的组织微环境(niches)来驱动T细胞异质性?这些问题对于理解前列腺免疫、慢性前列腺炎以及前列腺癌免疫治疗具有重要意义。
本研究首次系统性地利用遗传小鼠模型、功能遗传学、scRNA-seq和10x Xenium空间转录组学,全面解析了前列腺Trm细胞的形成、功能、异质性及其与空间微环境的关系,为前列腺免疫学建立了全新的研究框架。
二、研究设计概览
分析维度 | 技术/模型 | 核心目标 |
|---|---|---|
Trm形成与表征 | P14 TCR转基因T细胞 + LCMV急性感染 | 验证前列腺生成长寿命Trm细胞 |
组织驻留验证 | 联体共生(Parabiosis)实验 | 确认细胞真正驻留而非再循环 |
功能保护验证 | 异源二次感染 + 低剂量抗CD8α清除 | 评估Trm对再感染的保护能力 |
信号通路解析 | TGFβR2/AR条件性敲除 + IL-15 KO + IL-7R阻断 | 鉴定驱动Trm分化的关键细胞因子 |
瘤内异质性 | scRNA-seq (小鼠+人前列腺CD8+ T细胞) | 揭示Trm亚群的转录异质性 |
空间定位 | 10x Xenium (480基因panel, 亚细胞分辨率) | 将T细胞表型映射到离散组织微环境 |
人类验证 | 人前列腺活检多重免疫荧光 | 验证小鼠发现在人类中的保守性 |
三、主要发现
3.1 急性病毒感染生成长寿命的前列腺Trm细胞
研究者将P14 CD8+ T细胞(识别LCMV GP33-41肽段)过继转移至受体小鼠,随后进行LCMV感染,并在感染后多个时间点追踪前列腺中的T细胞动态。
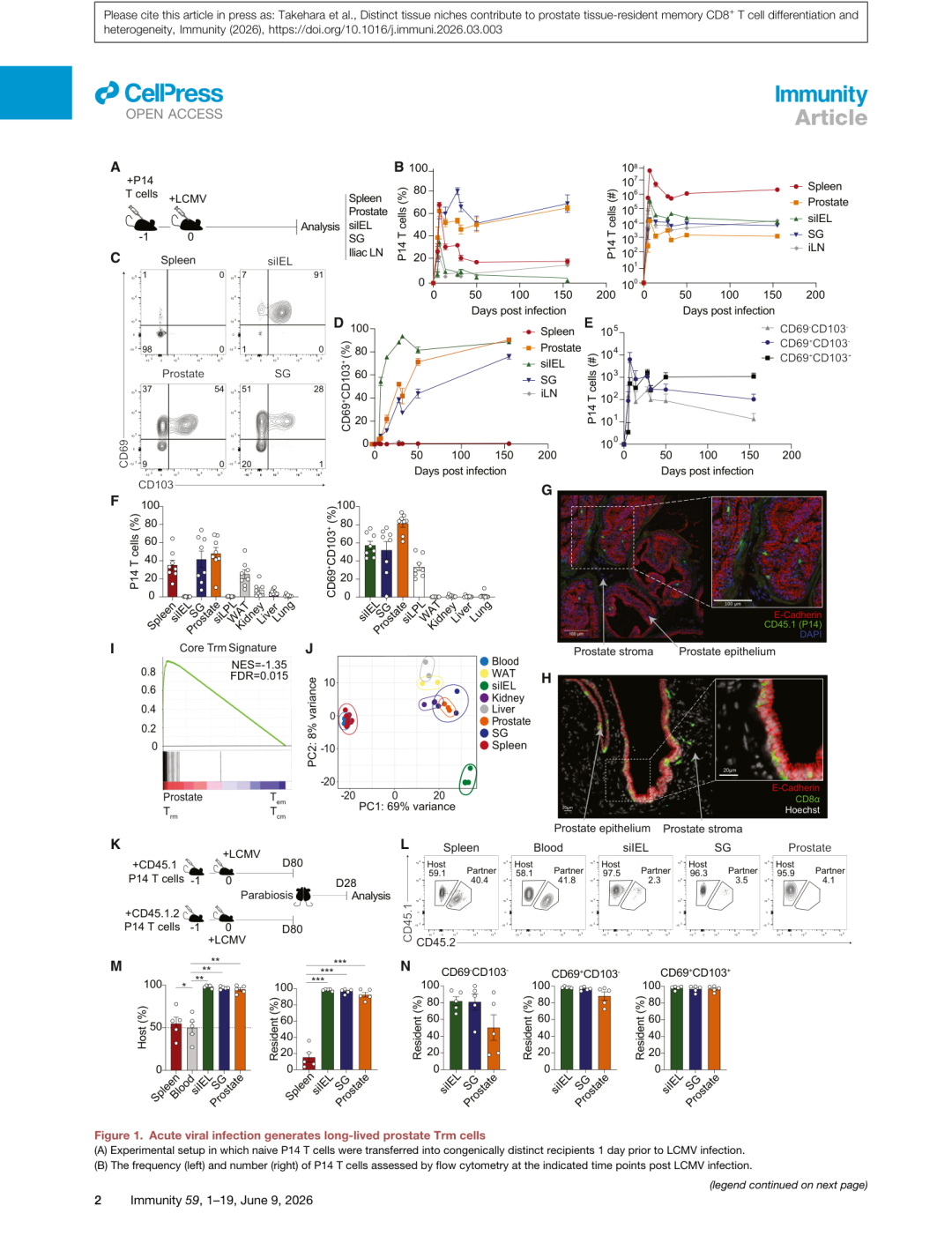
Figure 1: 前列腺Trm细胞的特征鉴定
Figure 1: 前列腺Trm细胞的特征鉴定
▲ Figure 1 | 急性病毒感染生成长寿命的前列腺Trm细胞。 (A) 实验设计;(B) 前列腺P14 T细胞频率和数量的时间动态;(C-D) CD69/CD103表达谱;(E) CD69+CD103+亚群的绝对数量稳定性;(G-H) 小鼠和人前列腺CD8+ T细胞的组织定位(富集于上皮区域);(I) GSEA分析显示前列腺Trm富集核心Trm基因签名;(J) PCA分析展示前列腺Trm与其他组织Trm的转录组比较;(K-N) 联体共生实验证实组织驻留特性。
核心发现:
- 前列腺中建立了一个稳定的长寿命Trm群体,可持续存在超过500天(几乎小鼠的终生),占前列腺总CD8+ T细胞的约40%
- CD69+CD103+共表达在感染后150天达峰(约80%),并保持稳定
- 联体共生实验确认前列腺T细胞以宿主来源为主体(>95%),CD69+细胞的驻留率达90-100%
- 免疫组化和显微镜显示:前列腺Trm细胞富集于上皮区域,此特征在人类前列腺样本中同样存在
- 转录组分析显示前列腺Trm细胞在PCA中与肾脏和唾液腺Trm最为接近,同时具有前列腺特异性基因表达(如Ccl6、Cxcr4、P2rx7以及雄激素应答基因Insig1、Acsl3)
值得注意的是,尽管前列腺和唾液腺Trm细胞表达最高水平的雄激素受体(AR),但AR条件性敲除的影响并非前列腺特异性的,而且雌性来源的T细胞在前列腺中形成了同等数量的Trm细胞。这表明前列腺组织环境而非性别二态性决定了Trm形成和表型。
3.2 前列腺Trm细胞保护宿主抵御再感染
为了评估前列腺Trm的功能保护能力,研究者采用了精巧的实验设计:先用Lm-GP33初次感染生成记忆,再用低剂量抗CD8α清除循环CD8+ T细胞(但不影响组织驻留T细胞),最后用LCMV进行异源再挑战。
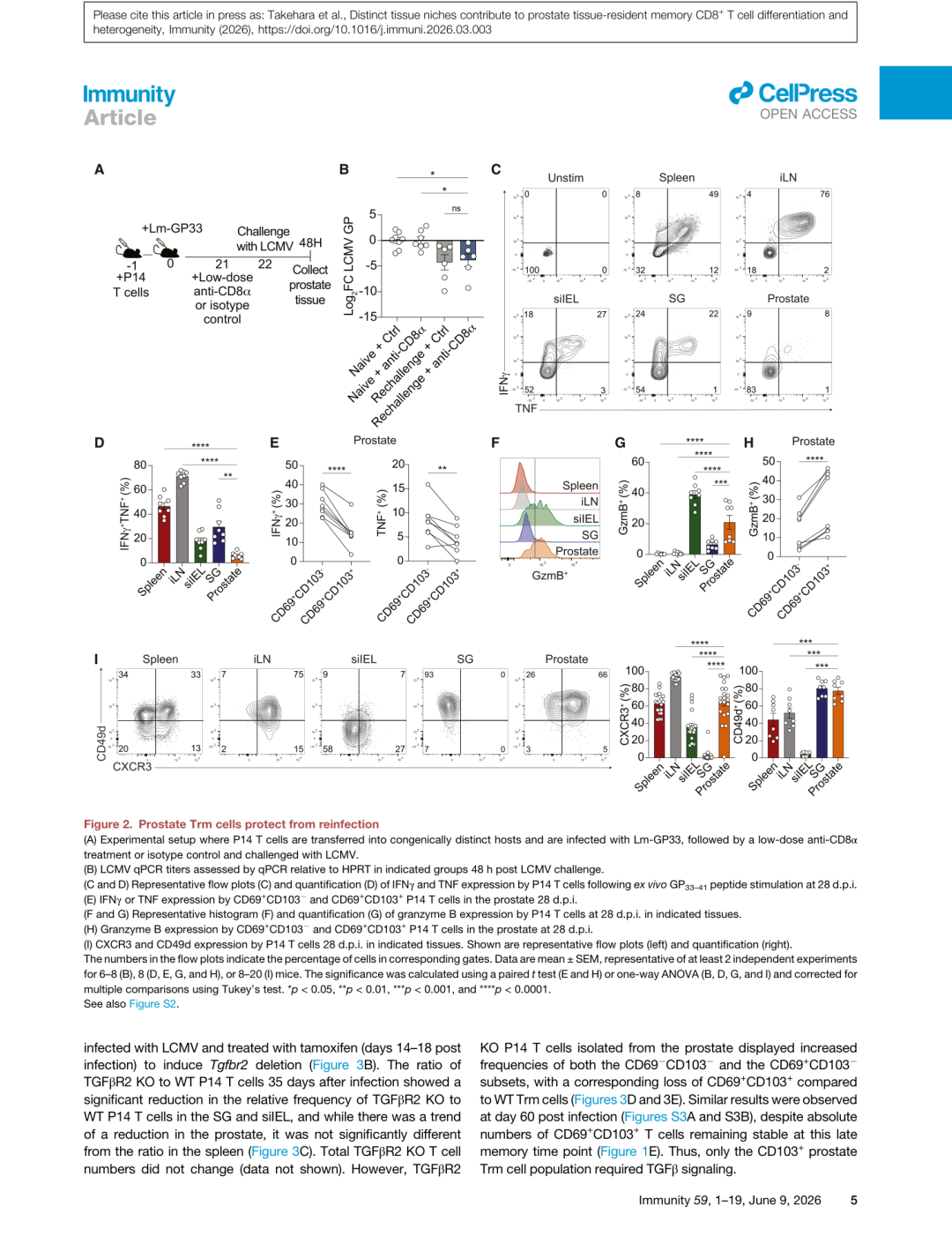
Figure 2: 前列腺Trm的功能表征
Figure 2: 前列腺Trm的功能表征
▲ Figure 2 | 前列腺Trm细胞保护主体抵御再感染。 (A) 实验设计示意;(B) LCMV病毒滴度定量;(C-E) IFNγ和TNF细胞因子产生能力;(F-H) Granzyme B表达定量;(I) CXCR3和CD49d表达。
关键发现:
- 清除循环CD8+ T细胞不影响病毒保护能力,证明Trm本身足以抵御再感染
- 前列腺Trm产生的细胞因子少于其他组织的Trm,但并非"功能失调"
- 功能亚群按CD103表达分化:
- CD69+CD103−:产生更多IFNγ和TNF
- CD69+CD103+:表达更多Granzyme B(细胞毒性更强)
- 前列腺Trm保留了CXCR3(约80%)和CD49d/VLA-4的表达——这在唾液腺和小肠Trm中不常见
3.3 TGFβ信号维持CD103+亚群并抑制Trm效应功能
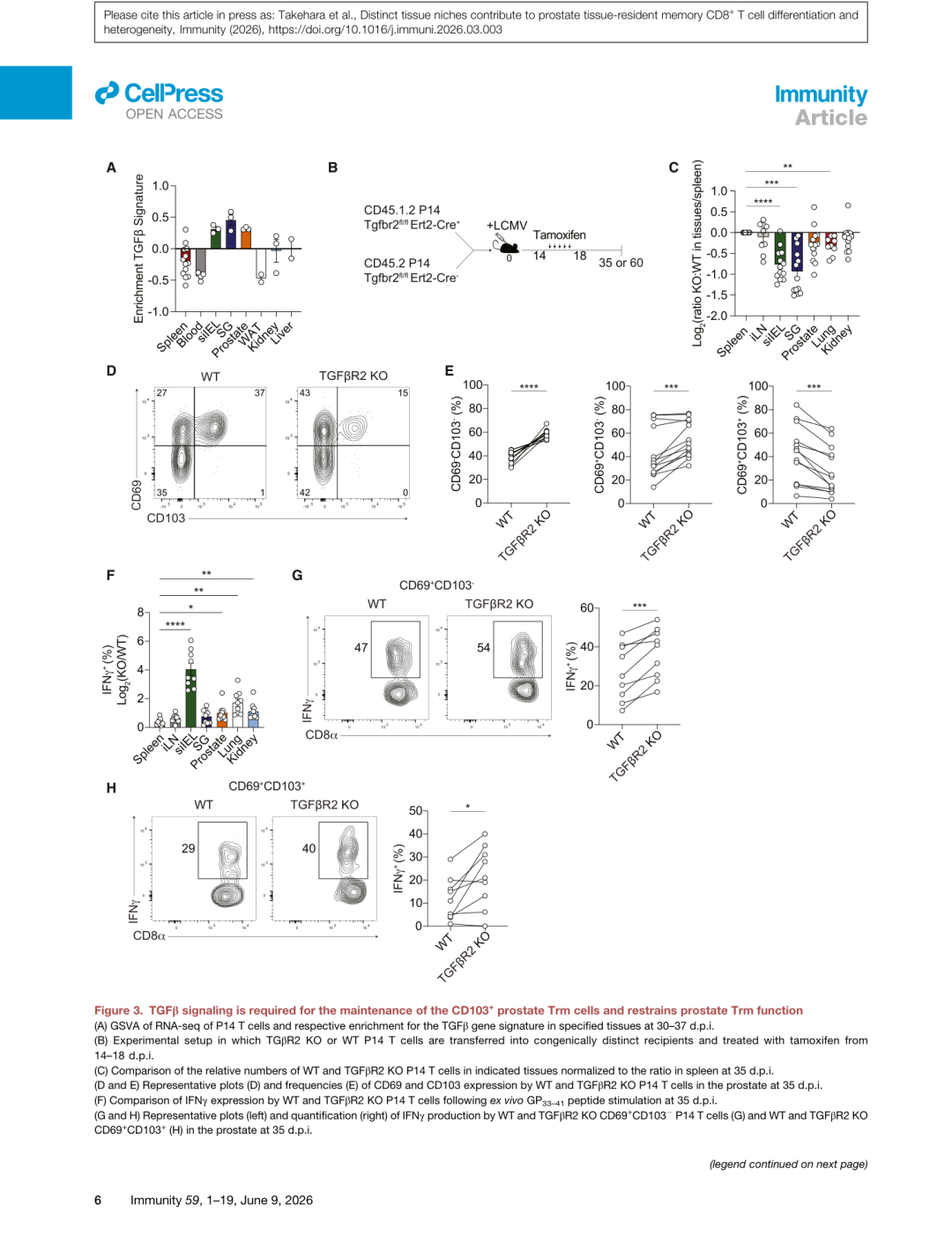
Figure 3: TGFβ对前列腺Trm的调控
Figure 3: TGFβ对前列腺Trm的调控
▲ Figure 3 | TGFβ信号是维持CD103+前列腺Trm细胞和抑制功能的必需条件。 (A) TGFβ基因签名富集分析;(B) 条件性敲除实验设计(他莫昔芬诱导Tgfbr2缺失);(C-E) TGFβR2 KO的表型变化;(F-H) TGFβR2缺失导致IFNγ产生增加。
研究者利用他莫昔芬诱导的条件性Tgfbr2敲除系统(在记忆形成阶段第14-18天删除),发现:
- TGFβR2缺失导致前列腺中CD69+CD103+亚群显著减少,同时CD69−CD103−和CD69+CD103−亚群增加
- TGFβR2 KO的Trm细胞IFNγ产生增加约2倍,TNF增加约1.4倍——这一增强效应同时见于CD103+和CD103−亚群
- 过表达核心Trm转录因子Runx3可将前列腺中CD69+CD103+的频率从30%提高至约60%
这一发现具有重要的临床转化意义:TGFβ在前列腺上皮中高表达,它既维持CD103+Trm的组织滞留,又限制了Trm的效应功能。前列腺作为生殖器官,可能通过TGFβ介导的免疫抑制来平衡抗感染与避免炎症损伤(前列腺炎与男性不育密切相关),这是一种适应性的组织免疫调节机制。
3.4 IL-7和IL-15协同维持前列腺Trm细胞
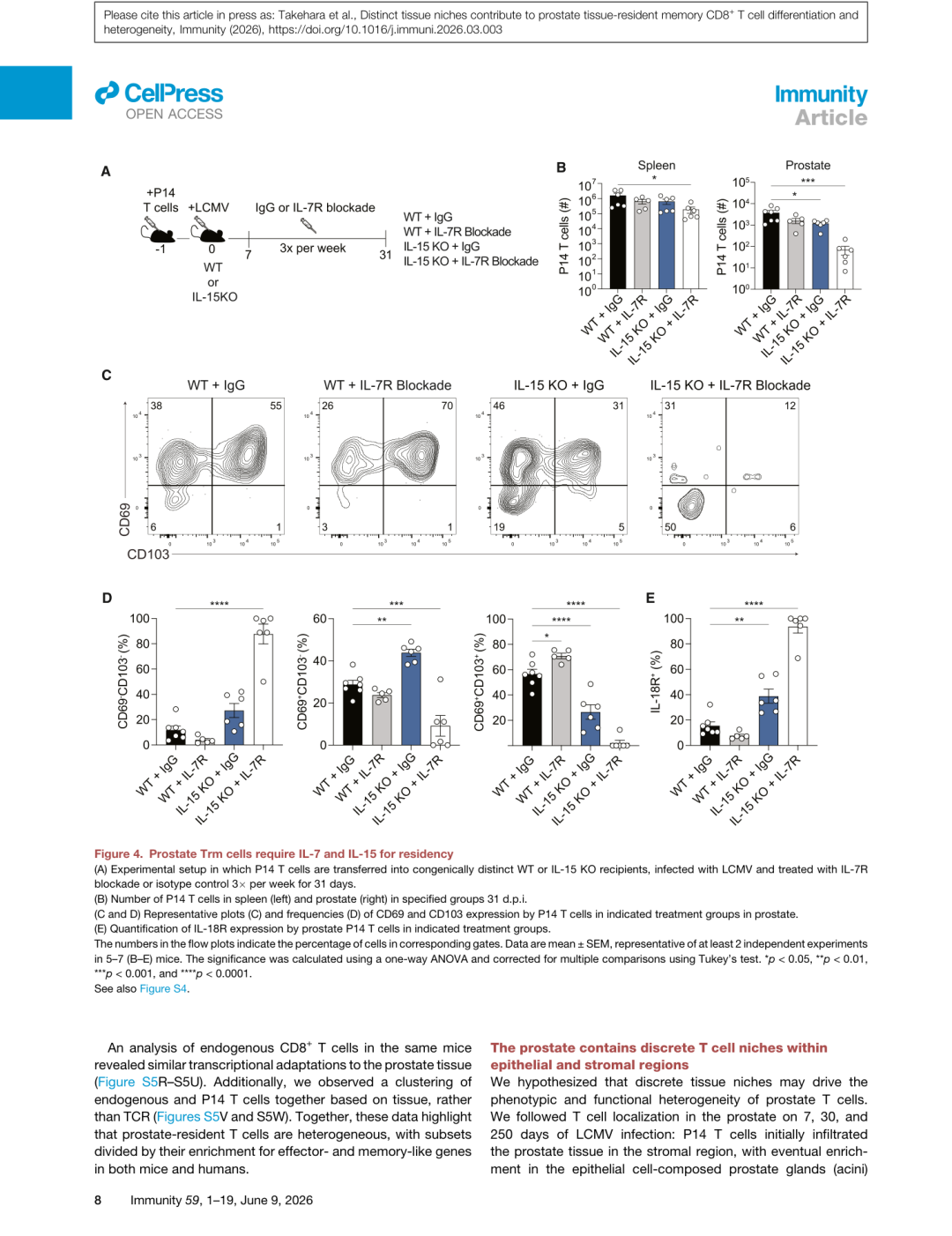
Figure 4: IL-7/IL-15对前列腺Trm的维持
Figure 4: IL-7/IL-15对前列腺Trm的维持
▲ Figure 4 | 前列腺Trm细胞需要IL-7和IL-15维持驻留。 (A) 实验设计(IL-15 KO受体 + IL-7R阻断抗体);(B) P14 T细胞数量变化;(C-D) CD69/CD103表型变化;(E) IL-18R表达。
通过将P14 T细胞转入IL-15 KO受体并联合IL-7R阻断抗体处理:
- 双重缺失导致前列腺Trm数量下降约50倍
- 单独IL-15缺失导致CD69+CD103+频率下降2.5倍
- 单独IL-7R阻断对CD103+Trm数量无显著影响,提示IL-7和IL-15可以互相补偿
- 残存的T细胞主要是**IL-18R+**的,提示IL-18可能是第三条维持通路
3.5 scRNA-seq揭示前列腺Trm的异质性亚群
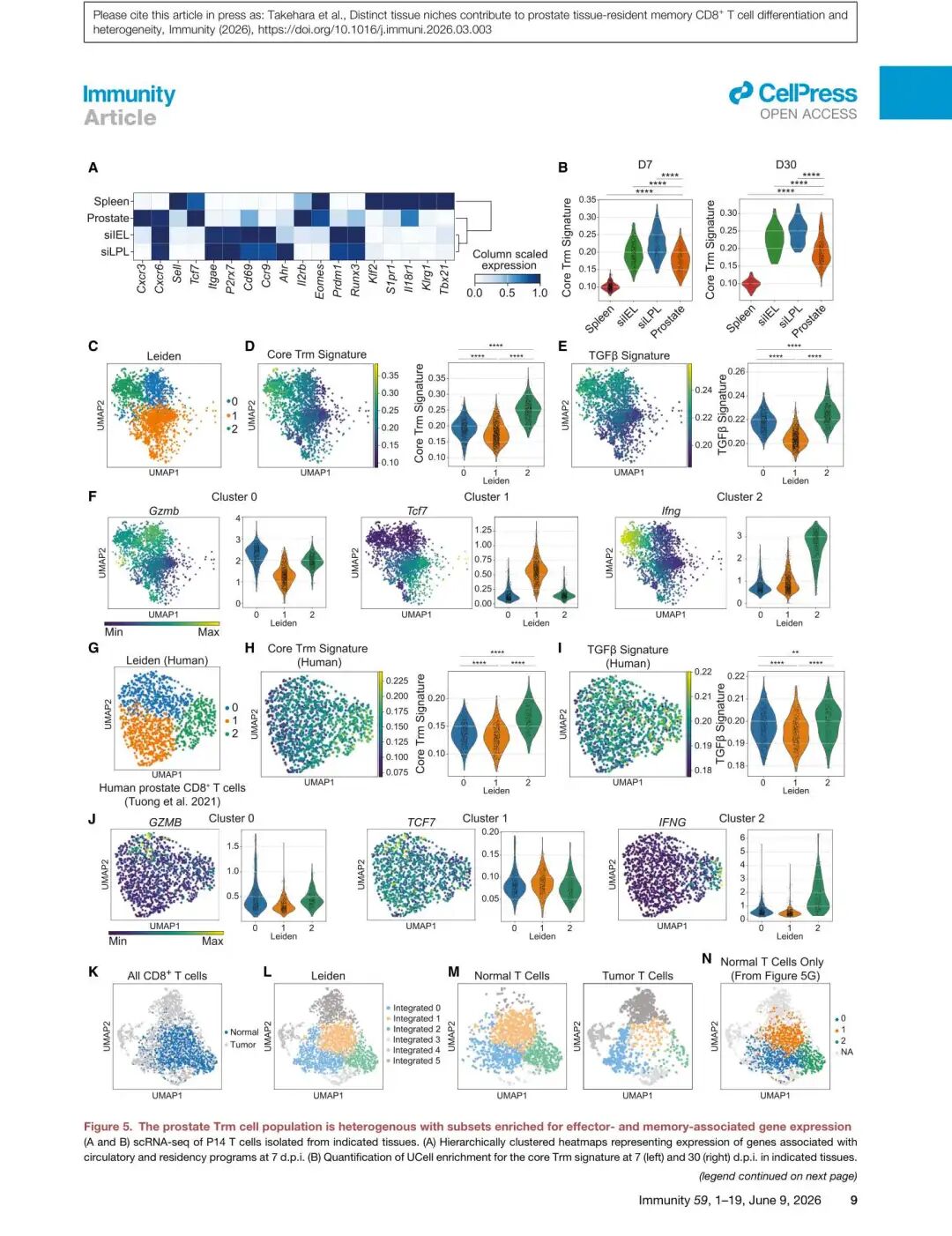
Figure 5: 前列腺Trm的scRNA-seq异质性分析
Figure 5: 前列腺Trm的scRNA-seq异质性分析
▲ Figure 5 | 前列腺Trm群体的异质性——效应样和记忆样亚群。 (A) 循环/驻留基因表达热图;(B) 核心Trm签名富集评分;(C-F) 小鼠前列腺scRNA-seq Leiden聚类与标志基因;(G-J) 人类健康前列腺CD8+ T细胞scRNA-seq类似的三亚群模式;(K-N) 前列腺癌中同样存在的Trm亚群。
scRNA-seq在小鼠前列腺P14 T细胞(感染后34天)中鉴定了三个转录组不同的亚群:
亚群 | 核心特征 | 关键基因 | 功能定位 |
|---|---|---|---|
Cluster 0 | 细胞毒效应型 | Gzmb↑, Gzmk↑, Itgae+ | 高TGFβ签名,高杀伤能力 |
Cluster 1 | 记忆样 | Il18r1↑, Tcf7↑, Klf2↑, Il7r↑ | 循环记忆特征,低Trm签名 |
Cluster 2 | 细胞因子效应型 | Ifng↑, Tnf↑, Xcl1↑, Itgae+ | 最高核心Trm签名 |
跨物种保守性: 人类健康前列腺CD8+ T细胞(来自公开scRNA-seq数据36)同样显示出高度相似的三亚群结构:
- Cluster 0和2富集细胞毒或细胞因子效应基因
- Cluster 1富集记忆相关基因(TCF7、IL7R)
- 小鼠各cluster的基因签名可以分别投射到对应的人类cluster上
更重要的是,前列腺癌组织中也存在这些Trm亚群,提示肿瘤中包含预先存在的Trm细胞。
3.6 10x Xenium空间转录组揭示前列腺的离散组织微环境
这是本研究最精彩的部分。研究者设计了一个480基因的Xenium面板(在此前小肠350基因面板基础上扩展130个前列腺/细胞因子/免疫相关基因),在LCMV感染后第7天和第30天的小鼠前列腺中进行亚细胞分辨率的空间转录组分析。
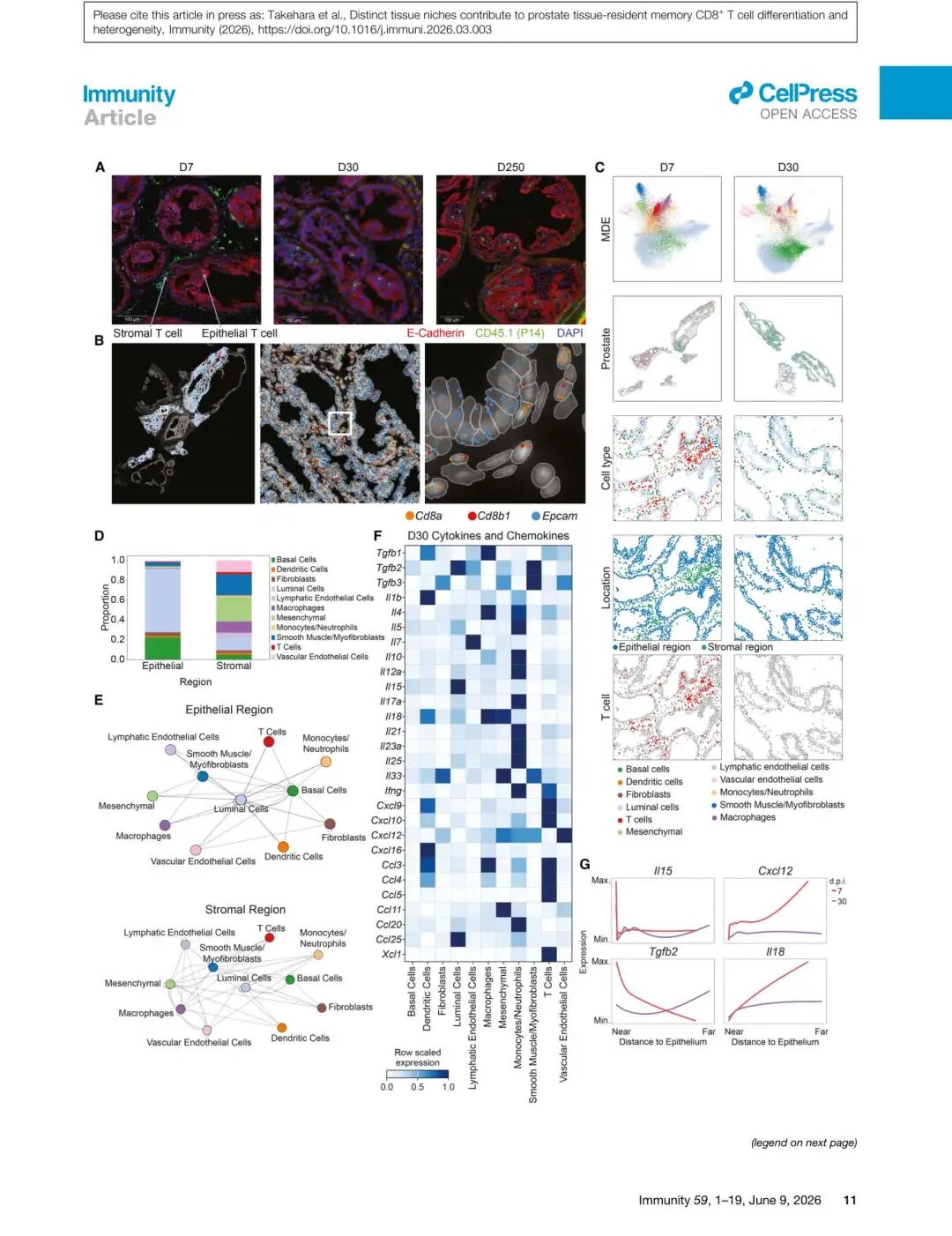
Figure 6: 前列腺的离散上皮和基质组织微环境
Figure 6: 前列腺的离散上皮和基质组织微环境
▲ Figure 6 | 前列腺包含离散的上皮和基质组织微环境。 (A) 感染后7/30/250天的前列腺共聚焦显微镜;(B) Xenium数据概览——细胞类型定位和转录本检测;(C) 联合MDE降维和原位空间定位展示11种细胞类型的分布;(D) 上皮/基质区域的细胞类型组成;(E) 细胞互作网络;(F) 各细胞类型的细胞因子/趋化因子表达热图;(G) 关键细胞因子沿上皮距离的梯度分布。
空间分析揭示了两个功能性微环境:
上皮微环境(Epithelial niche):
- 主要由腔上皮细胞和基底上皮细胞组成
- 富集Tgfb2和Il15转录本——两种维持CD103+ Trm的关键细胞因子
- 上皮细胞同时表达TGFβ激活所需的整合素亚基αv(Itgav)和β6(Itgb6)
- 标记基因:Cdh1(E-cadherin)
基质微环境(Stromal niche):
- 主要由血管内皮细胞、平滑肌细胞、巨噬细胞和间充质细胞组成
- 富集Cxcl12(来源于血管内皮、单核/中性粒细胞和肌成纤维细胞)
- 富集Il18(来源于树突状细胞、间充质细胞和巨噬细胞)
- 标记基因:Vcam1
细胞因子梯度的关键发现:
- Il15和Tgfb2在上皮区域浓度最高,随距上皮距离增加而递减
- Cxcl12和Il18随距上皮距离增加而递增,在基质区域最高
3.7 Trm异质性映射到空间离散的微环境信号
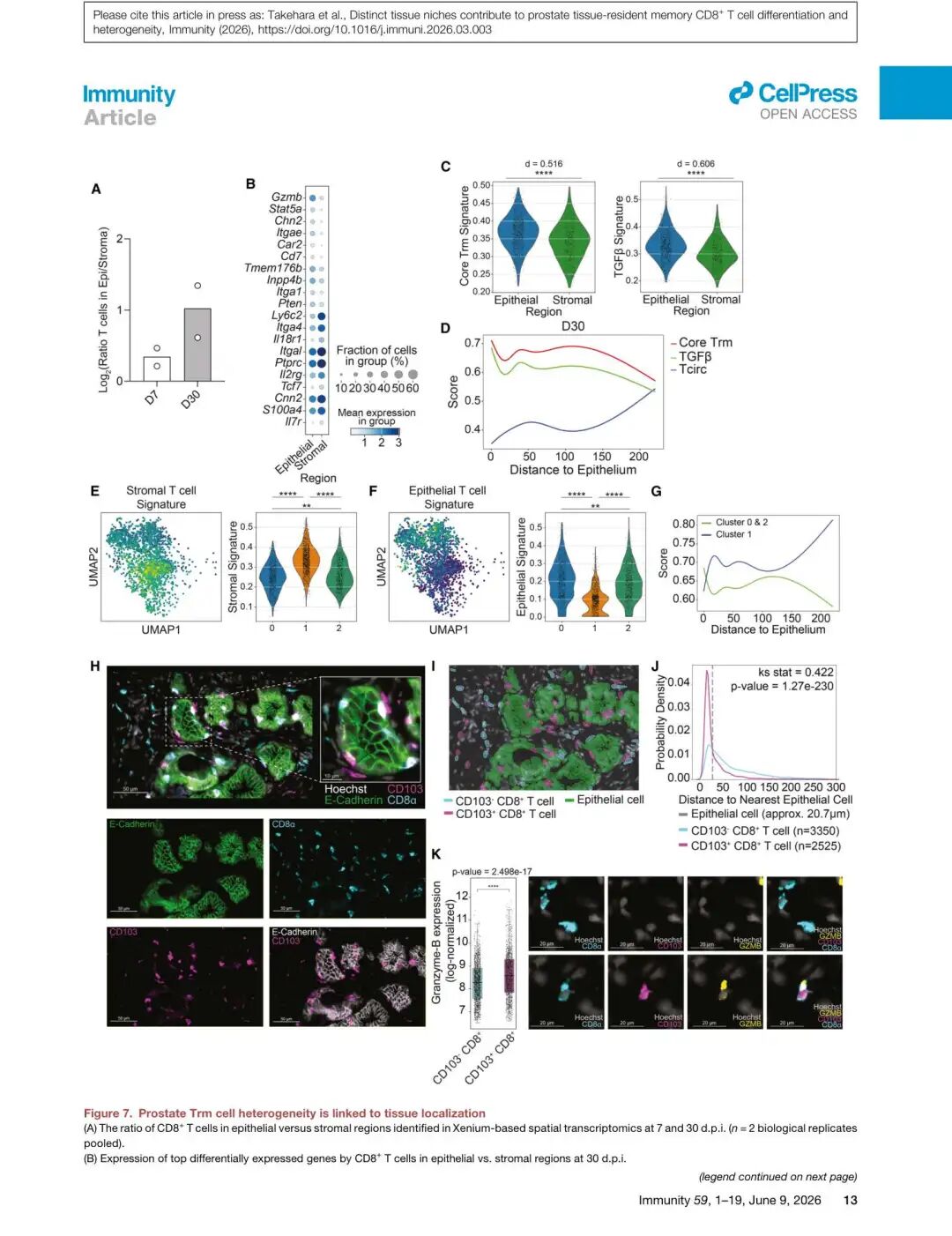
Figure 7: Trm异质性与组织定位的关联
Figure 7: Trm异质性与组织定位的关联
▲ Figure 7 | 前列腺Trm细胞异质性与组织定位紧密关联。 (A) 上皮/基质区域CD8+ T细胞比例随时间变化;(B) 上皮vs基质区域T细胞的差异表达基因;(C) 核心Trm和TGFβ签名的空间分布;(D) 沿上皮距离的签名富集趋势;(E-F) 基质/上皮空间签名投射回scRNA-seq聚类;(G) scRNA-seq cluster签名的空间分布;(H-K) 人类前列腺CD103+/CD103− CD8+ T细胞的空间分布验证。
将空间转录组与scRNA-seq整合后,研究者建立了Trm异质性的空间框架:
上皮区域的T细胞(效应样):
- 富集Itgae(CD103)、Gzmb和Itga1
- 高度富集核心Trm签名和TGFβ签名
- 对应scRNA-seq中的Cluster 0和Cluster 2
基质区域的T细胞(记忆样):
- 富集Tcf7、Il7r、Il18r1和Itga4(CD49d)
- 低Trm签名,高循环记忆签名
- 对应scRNA-seq中的Cluster 1
空间连续性: T细胞的基因表达沿距上皮距离呈连续梯度变化:
- 越接近上皮→核心Trm签名和TGFβ签名越高
- 越远离上皮→循环记忆签名越高
人类验证: 多重免疫荧光分析人类前列腺活检样本显示:
- CD103+ CD8+ T细胞富集于上皮细胞附近
- CD103+ T细胞表达更高水平的Granzyme B
- 这与小鼠的空间模式完全一致
临床转化的关键启示:前列腺癌中也存在相似的Trm亚群和人类前列腺中TGFB2由上皮细胞高表达的模式。当前列腺发生恶变时,这些细胞因子梯度的扰动可能影响驻留T细胞的表型和功能。这为前列腺癌免疫治疗的设计提供了重要的微环境靶点线索。
四、讨论与临床意义
4.1 前列腺免疫平衡的独特机制
前列腺作为外分泌腺和屏障组织,必须在维持生殖功能(减少炎症损伤)和限制病原体复制之间取得平衡。前列腺炎与男性不育高度相关,因此前列腺通过TGFβ介导的效应功能抑制可能是一种适应性特征——在最高效的杀伤能力和最小的组织损伤之间寻找平衡点。
4.2 空间微环境决定T细胞命运
本研究最重要的概念性贡献在于:离散的组织微环境通过局部化的细胞因子梯度塑造了单个器官内T细胞的功能异质性。上皮niche(高IL-15/TGFβ)驱动持久的、细胞毒性的CD103+ Trm;基质niche(高CXCL12/IL-18)支持更具记忆特征的、表达TCF7的CD103− T细胞。
4.3 CD103−前列腺T细胞的长期持续
与小肠Trm不同,前列腺中存在一群长期持续的CD103−T细胞,它们表达循环记忆相关基因但不表达CX3CR1(排除Tpm特征),并通过CXCR3和CD49d维持组织滞留。这一亚群定位于基质区域(VCAM1+间充质细胞附近),可能通过VLA-4/VCAM1相互作用实现组织驻留。
五、技术方法学亮点
- Xenium 480基因定制面板设计:在前人小肠研究350基因面板基础上扩展130个前列腺/细胞因子/免疫基因,实现了对前列腺微环境的全面表征
- 细胞因子距离梯度分析:利用广义加性模型(GAM)拟合细胞因子表达沿"距上皮距离"轴的趋势曲线,将空间数据转化为可解读的生物学梯度
- 空间-转录组交叉验证:从空间数据提取上皮/基质区域特异性基因签名,投射回scRNA-seq聚类进行双向验证——这种分析范式值得广泛推广
- 精巧的功能遗传学设计:利用条件性敲除(TGFβR2, AR)、基因过表达(Runx3)和细胞因子操控(IL-15 KO + IL-7R阻断)系统化地解析每条信号通路的贡献
六、总结与展望
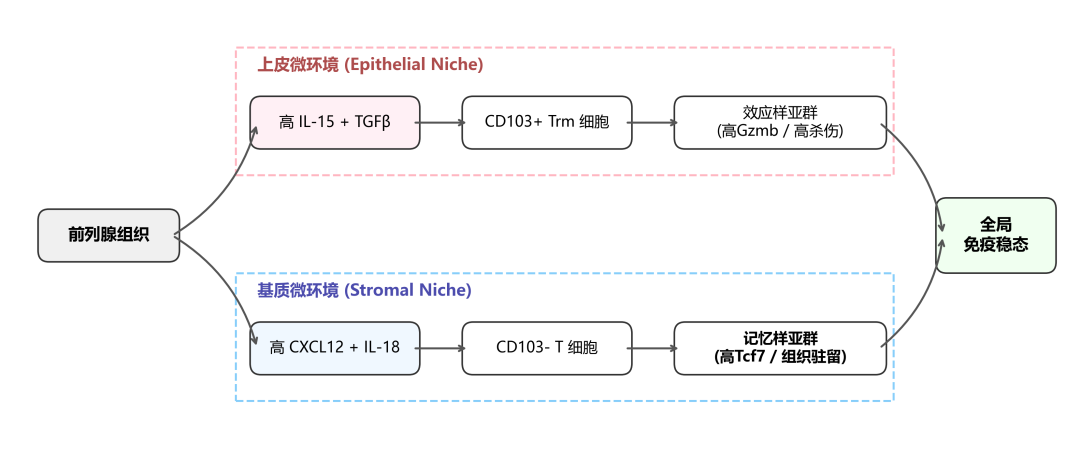
前列腺Trm细胞空间分化机制
前列腺Trm细胞空间分化机制
本研究的核心贡献:
- 首次全面表征前列腺Trm细胞——长寿命(>500天)、具有核心驻留特征、保护性但功能受限
- 鉴定了前列腺Trm的关键调控因子——TGFβ维持CD103+并抑制效应功能;IL-15和IL-7协同维持Trm存活
- 建立了"空间微环境-T细胞命运"的对应框架——上皮niche产生效应型Trm,基质niche维持记忆型T细胞
- 跨物种验证了这一框架在人类前列腺中的保守性——小鼠发现在人类健康前列腺和前列腺癌中均成立
未来方向:
- 慢性前列腺炎和前列腺癌中Trm表型如何改变?
- CXCL12/CXCR4轴是否参与基质T细胞的驻留维持?
- 前列腺癌免疫治疗是否可以通过调控TGFβ来增强Trm效应功能?
- 这一"空间微环境决定Trm异质性"的框架是否广泛适用于其他组织?
本研究建立了一个从功能遗传学→转录组学→空间组学→人类验证的完整研究范式,为理解组织驻留免疫的空间调控提供了方法学模板。对于从事肿瘤免疫、空间转录组学和T细胞生物学的研究者,这篇文章值得深入学习。
参考文献:Takehara KK, Monell A, et al. Distinct tissue niches contribute to prostate tissue-resident memory CD8+ T cell differentiation and heterogeneity. Immunity 59, 1–19 (2026). DOI: 10.1016/j.immuni.2026.03.003
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-08,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

